Asherman-Syndrom
| Klassifikation nach ICD-10 | |
|---|---|
| N85.6 | Intrauterine Synechien |
| ICD-10 online (WHO-Version 2019) | |
Das Asherman-Syndrom, auch als Fritsch-Syndrom oder Fritsch-Asherman-Syndrom bekannt, bezeichnet Verwachsungen beziehungsweise Verklebungen (Synechien) der Gebärmuttervorder- und -rückwand,[1] die häufig traumatisch bedingt ist, meist durch eine Kürettage. Folgen können eine Amenorrhoe, Hypomenorrhoe, habituelle Aborte und eine sekundäre Sterilität sein.
Das Krankheitsbild wurde nach den Erstbeschreibern Joseph Gustav Asherman (1889–1968), einem tschechisch-israelischen Gynäkologen und Heinrich Fritsch (1844–1915), einem deutschen Gynäkologen, benannt.[2][3] Einzelfälle wurden bereits früher durch Ernst Wertheim (1864–1920), Otto Ernst Küstner (1849–1931), Gustav Veit (1824–1903) und anderen beschrieben.
Ursachen
Verwachsungen (Synechien) und Narbengewebe (Fibrosen) können entstehen, wenn die Basalschicht der Gebärmutterschleimhaut während eines operativen Eingriffs in ihrer Tiefe verletzt wurde. Da in und nach einer Schwangerschaft die Gebärmutterschleimhaut besonders empfindlich ist, besteht hier ein erhöhtes Risiko.[4]
Als weitere Ursachen werden alleinige Entzündungen der Gebärmutterschleimhaut (Endometritis), wie beispielsweise bei genitalen Tuberkulose diskutiert.[5][6]
Nach Gebärmuttereingriffen außerhalb der Schwangerschaft sind intrauterine
Adhäsionen viel seltener und kommen dabei vor allem nach hysteroskopischen Eingriffen vor.[4]
Folgen

Das Asherman-Syndrom ist bei leichten Adhäsionen seltener, bei schweren Verwachsungen öfter Ursache einer Unfruchtbarkeit[1] führt jedoch häufig zu Amenorrhoe, Hypomenorrhoe, sowie Dysmenorrhoe und habituellen Aborten. Nach einer hysteroskopischen Durchtrennung von leichten bis mittelschweren Synechien kommt es in 3–4 % der Fälle zu einem Rezidiv. Bei schweren intrauterinen Adhäsionen muss mit einer Rezidivhäufigkeit von bis zu 63 % gerechnet werden.[4]
Diagnostik
Im Ultraschall lassen sich Hinweise auf das Krankheitsbild finden. Das Endometrium lässt sich meist nur mit Schwierigkeit identifizieren. Je nach Lokalisation der Verwachsungen kann ggf. auch eine Hämatometra darstellbar sein.
Im Vergleich zur Hysteroskopie, welche heute die Standardmethode zur Diagnostik darstellt, hat die transvaginale Sonografie jedoch nur eine Sensitivität von 52 % und eine Spezifität von 11 % beim Nachweis von intrauterinen Verwachsungen.[4] In der dreidimensionalen Ultraschalluntersuchung (3D-Sonografie) zeigt sich in den betroffenen Bereichen ein vermindertes Endometriumvolumen.[7]
Vor einem Eingriff spielt die Transvaginalsonographie dennoch eine wichtige Rolle. Patientinnen, bei welchen ultrasonographisch hinter einem obstruktiven Bereich Endometrium nachgewiesen werden kann, haben eine größere Wahrscheinlichkeit erfolgreich behandelt zu werden.[4] Die Gebärmutterspiegelung kann im Vergleich zu allen anderen Verfahren viel genauer und präziser Vorhandensein, Ausmaß und Grad von intrauterinen Adhäsionen darstellen und ermöglicht eine gute Beurteilung der Qualität des restlichen Endometriums. Sie gilt daher als Methode der Wahl bei der Diagnostik von intrauterinen Adhäsionen.
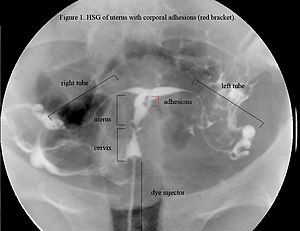
Sie hat damit die Hysterosalpingografie praktisch vollständig abgelöst, bei der sich Füllungsdefekte des Cavum uteri, der Tubenenden oder der Tubenostien, je nach Ausdehnung und Lokalisation der Adhäsionen darstellen ließen. Sie ermöglichte es jedoch nicht, eine klare Aussage zu treffen, was die Ursache für diese Füllungsdefekte ist.[4]
Prophylaxe
Bei Ausschabungen in oder nach einer Schwangerschaft werden ausschließlich stumpfe Instrumente (Küretten) benutzt und es wird nur mit sanftem Druck gearbeitet. Etwas weniger Risiko birgt eine Absaugung, sodass die Saugkürettage, wenn möglich bevorzugt werden sollte.
Bei der Indikationsstellung von intrauterinen Eingriffen, wie beispielsweise hysteroskopischen Myomresektionen, sollte auch immer das Risiko eines Asherman-Syndroms mit eingeschlossen werden.[4]
Therapie
Die Hysterotomie (Eröffnung der Gebärmutter) mit Lösen der Verwachsungen per Bauchschnitt (Laparotomie) ist heute nur noch in Ausnahmefällen gerechtfertigt und wurde praktisch vollständig von der hysteroskopischen Therapie abgelöst.
Dabei werden die Verwachsungen instrumentell, teilweise unter Einsatz elektrochirurgischer Methoden, gelöst. Der Einsatz eines Lasers scheint keine Vorteile zu bringen.[8]
Zur Prophylaxe erneuter Verwachsungen werden hormonelle Behandlungen zur Stimulation der Gebärmutterschleimhaut, sowie Barrieremethoden, wie Hyaluronsäure oder Intrauterinpessare eingesetzt.[8][4]
Des Weiteren gibt es Forschungen im Bereich der Stammzelltherapie, bei der verbliebene endometriale (mesenchymale) aus der Basalis oder hämatopoetische Stammzellen aus dem Knochenmark entnommen, vermehrt und eingesetzt werden. Die Stammzellen sorgen für das Wachstum der darüberliegenden Gebärmutterschleimhaut.[9][8][10]
Literatur
- J.G. Asherman: Syndrome d'Asherman. In: Rev Fr Gynecol Obstet. 61 (1966), S. 542–544, PMID 5940503
- J.G. Asherman: Intrauterine adhesions. In: Bull Fed Soc Gynecol Obstet Land Fr. 4 (1952), S. 807–814.
- S. Friedler, E. J. Margalioth, I. Kafka, H. Yaffe: Incidence of post-abortion intra-uterine adhesions evaluated by hysteroscopy - a prospective study. In: Hum Reprod. 8 (1993), S. 442–444.
- W. Pschyrembel, G. Strauss, E. Petri: Praktische Gynäkologie. 5. Auflage. Walter de Gruyter, Berlin 1991, ISBN 3-11-003735-1, S. 517–519.
- Rebecca Deans, Jason Abbott: Review of Intrauterine Adhesions. In: J Minim Invasive Gynecol. 17 (2010), S. 555–569, PMID 20656564, doi:10.1016/j.jmig.2010.04.016
- Collin Smikle, Shailesh Khetarpal: Asherman Syndrome. StatPearls Publishing, Treasure Island (Florida) 2019, PMID 28846336
Weblinks
- Asherman's syndrome auf whonamedit.com
- Corinna Maria Dartenne: Das Asherman-Syndrom - ein kaum bekanntes Risiko. auf: Spiegel Online. 6. April 2003, zuletzt abgerufen am 17. Februar 2011
Einzelnachweise
- ↑ a b Baltzer u. a.: Praxis der Gynäkologie und Geburtshilfe. Thieme, Stuttgart 2004, S. 406f.
- ↑ J. G. Asherman: Amenorrhoea traumatica (atretica). In: J Obstet Gynecol Br Emp. 1948, S. 23–30.
- ↑ H. Fritsch: Ein Fall von völligem Schwund der Gebärmutterhöhle nach Auskratzung. In: Zentralbl Gynäkol. 1894; 18, S. 1337–1342.
- ↑ a b c d e f g h Michael D. Mueller: Asherman-Syndrom: Ursachen und Behandlung. Frauenheilkunde aktuell 23/2/2014, S. 4–12, online
- ↑ Joachim W. Dudenhausen: Frauenheilkunde und Geburtshilfe. Walter de Gruyter, 2002, ISBN 3110165627, S. 47
- ↑ Orhan Bukulmez, Hakan Yarali, Timur Gurgan: Total corporal synechiae due to tuberculosis carry a poor prognosis following hysteroscopic synechiolysis. Hum Reprod 14 (1999), S. 1960–1961, doi:10.1093/humrep/14.8.1960
- ↑ Werner Schmidt: Farbdopplersonographie in Gynäkologie und Geburtshilfe. Georg Thieme Verlag, 2000, ISBN 3131176210, S. 47–48
- ↑ a b c Alessandro Conforti, Carlo Alviggi, Antonio Mollo, Giuseppe De Placido, Adam Magos: The management of Asherman syndrome: a review of literature. Reprod Biol Endocrinol 11 (2013), PMID 24373209, doi:10.1186/1477-7827-11-118, S. 118–128
- ↑ Sapna Jain, Mayank Jain, Astha Gupta, Mannan Gupta, Poonam Verma: Role of Autologous Stem Cell Therapy in Asherman’s Syndrome and Thin Endometrium: A Case Series. Sch J Med Case Rep 5 (2017), doi:10.21276/sjmcr, S. 305–308
- ↑ Caroline E. Gargett, David L. Healy: Generating receptive endometrium in Asherman's Syndrome. J Hum Reprod Sci 4 (2011), S. 49–52, PMID 21772741