Longicatenamycine
Als Longicatenamycine bezeichnet man eine Gruppe von Antibiotika (auch S-520-Antibiotika genannt). Diese sind Naturstoffe mit antibakterieller Wirkung.
Vorkommen
Longicatenamycine werden aus der Fermentationsbrühe von Mikroorganismen gewonnen. So wurde die biotechnologische Gewinnung aus Streptomyces diastaticus beschrieben.[1][2][3]
Struktur
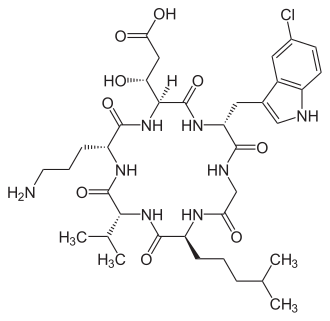
Longicatenamycine sind Cyclopeptide (Cyclohexapeptide). Die Struktur der Longicatenamycine wurde mittels Edman-Abbaureaktionen, Aminosäureanalysen und Kernresonanzspektroskopie aufgeklärt.[4][5] Die Longicatenamycine sind keine regulären Peptide des Primärstoffwechsels, vielmehr entstammen sie dem bakteriellen Sekundärstoffwechsel, der auch den Einbau ungewöhnlicher, nicht-proteinogener Aminosäuren erlaubt. So finden sich in den Longicatenamycinen die nicht-ribosomalen Aminosäuren 3-Hydroxyglutaminsäure, 5-Chlortryptophan und diverse Homoleucine.
Longicatenamycine unterscheiden sich an den Aminosäurepositionen 4 (Homoleucin), 5 (D-Valin bzw. D-Isoleucin) und 6 (D-Ornithin bzw. D-Lysin). Longicatenamycin A ist offenbar der Hauptmetabolit des Longicatenamycin-Komplexes.
Biologische Wirkung
Die Longicatenamycine sind wirksam gegen grampositive Krankenhauskeime wie z. B. gegen Staphylokokken und Enterokokken. Das In-vitro-Wirkniveau der natürlichen Longicatenamycine ist schlechter als das von Vancomycin.
Chemische Synthese
2008 wurde die erste Synthese von Longicatenamycin A beschrieben.[6]
Einzelnachweise
- ↑ J. Shoji, R. Sakazaki, J Antibiot. 1970, 23, 418–419.
- ↑ J. Shoji, R. Sakazaki, J. Antibiot. 1970, 23, 432–436.
- ↑ J. Shoji, R. Sakazaki, J. Antibiot. 1970, 23, 519–521.
- ↑ T. Shiba, Y. Mukunoki, J. Antibiot. 1975, 28, 561–566, PMID 1158781.
- ↑ T. Shiba, Y. Mukunoki, H. Akiyama, Tetrahedron Lett. 1974, 35, 3085–3086.
- ↑ F. von Nussbaum, S. Anlauf, C. Freiberg, J. Benet-Buchholz, J. Schamberger, T. Henkel, G. Schiffer, D. Häbich, ChemMedChem 2008, 3, 619–626, PMID 18246567.