Vitexin
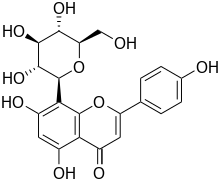
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Vitexin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C21H20O10 | |||||||||||||||
| Kurzbeschreibung |
gelbes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 432,38 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt |
260–263 °C[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Vitexin ist eine natürlich vorkommende chemische Verbindung. Als 8-C-Glucosyl-apigenin ist Vitexin ein Abkömmling des Apigenins, einem Pflanzenfarbstoff aus der Gruppe der Flavonoide. Das C-Glycosid ist strenggenommen kein echtes Glycosid, wird jedoch oft dieser Gruppe zugerechnet. Vitexin wirkt wie auch viele andere Flavonoide antioxidativ. In isolierter Form ist es ein kristallines gelbes Pulver.
Vorkommen

Vitexin kommt in der Passionsblume[5], in Brennnesseln[6] und häufig auch in Weißdornblättern[7] vor. Es wurde ferner in den Blättern einiger Bambussorten[8] sowie bei Knöterichen (Persicaria),[9] Roggen (Secale cereale)[10] und in den Samen des Bockshornklee (Trigonella foenum-graecum)[11] nachgewiesen.
Strukturverwandte
Ein Isomer des Vitexins ist das Isovitexin (Apigenin-6-C-Glucosid).
Einzelnachweise
- ↑ a b c Datenblatt Vitexin bei Sigma-Aldrich, abgerufen am 21. Mai 2017 (PDF).
- ↑ S. K. Kapoor, P. I. Ahmad, A. Zaman: Chemical constituents of ailanthus excelsa. In: Phytochemistry. Band 10, Nr. 12, 1971, S. 3333, doi:10.1016/S0031-9422(00)97424-7.
- ↑ Eintrag zu Vitexin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- ↑ Planta Medica. Vol. 43, 1981, S. 396.
- ↑ T. Dingermann, K. Hiller, G. Schneider, I. Zündorf: Schneider Arzneidrogen. 5. Auflage. Elsevier 2004, ISBN 3-8274-1481-4, S. 195.
- ↑ Quantitative determination of plant phenolics in Urtica dioica extracts by high-performance liquid chromatography coupled with tandem mass spectrometric detection. In: Food Chemistry. Band 143, 15. Januar 2014, ISSN 0308-8146, S. 48–53, doi:10.1016/j.foodchem.2013.07.097 (sciencedirect.com [abgerufen am 30. März 2018]).
- ↑ T. Dingermann, K. Hiller, G. Schneider, I. Zündorf: Schneider Arzneidrogen. 5. Auflage. Elsevier 2004, ISBN 3-8274-1481-4, S. 199.
- ↑ Y. Zhang, J. Jiao, C. Liu, X. Wu, Zhang, Y: Isolation and purification of four flavone C-glycosides from antioxidant of bamboo leaves by macroporous resin column chromatography and preparative high-performance liquid chromatography. In: Food Chemistry. 2007. doi:10.1016/j.foodchem.2007.09.037.
- ↑ R. Hänsel, K. Keller, H. Rimpler, G. Schneider (Hrsg.): Hagers Handbuch der Pharmazeutischen Praxis. Band 6: Drogen P–Z. 5. Auflage. Springer Berlin/ Heidelberg/ New York 1994, ISBN 3-540-52639-0, S. 74.
- ↑ R. Hänsel, K. Keller, H. Rimpler, G. Schneider (Hrsg.): Hagers Handbuch der Pharmazeutischen Praxis. Band 6: Drogen P–Z. 5. Auflage. Springer Berlin/ Heidelberg/ New York 1994, ISBN 3-540-52639-0, S. 649.
- ↑ R. Hänsel, K. Keller, H. Rimpler, G. Schneider (Hrsg.): Hagers Handbuch der Pharmazeutischen Praxis. Band 6: Drogen P–Z. 5. Auflage. Springer Berlin/ Heidelberg/ New York 1994, ISBN 3-540-52639-0, S. 1000.