Niob(V)-ethoxid
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
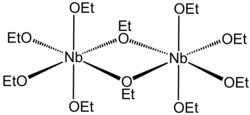
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Niob(V)-ethoxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C10H25NbO5 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 318,21 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
1,258 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,5160 (20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Niob(V)-ethoxid ist eine chemische Verbindung des Niobs aus der Gruppe der Ethanolate.
Gewinnung und Darstellung
Niob(V)-ethoxid kann durch Reaktion von Niob(V)-chlorid mit Ethanol in Gegenwart von Ammoniak gewonnen werden.[3][4] Die Verbindung kann auch elektrochemisch direkt aus Niob gewonnen werden.[5]
Eigenschaften
Niob(V)-ethoxid ist eine farblose bis bernsteinfarbene Flüssigkeit, die löslich in organischen Lösungsmitteln ist. In Wasser erfolgt Zersetzung.[1][2]
Verwendung
Niob(V)-ethoxid wird zur Herstellung von Niob(V)-oxid und Metallmischoxiden verwendet. Es wird auch für die Sol-Gel-Verarbeitung von Materialien eingesetzt, die Nioboxide und Metallmischoxide enthalten. Daneben dient es zur Herstellung ferroelektrischer Nanomaterialien, die aus Oxiden von Kalium, Silizium und Niob bestehen.[1]
Einzelnachweise
- ↑ a b c d e f g h i j k l Datenblatt Niobium(V) ethoxide, 99.999% (metals basis), Ta <500ppm bei AlfaAesar, abgerufen am 29. März 2020 (PDF) (JavaScript erforderlich).
- ↑ a b c
- ↑ Google Patents: US20020143200A1 - Process for preparing tantalum alkoxides and niobium alkoxides - Google Patents, abgerufen am 29. März 2020
- ↑ D. C. Bradley, B. N. Chakravarti, W. Wardlaw: 460. Normal alkoxides of quinquevalent niobium. In: Journal of the Chemical Society. 1956, S. 2381, Modul:Vorlage:Handle * library URIutil invalid.
- ↑ Ya-nan Cai, Sheng-hai Yang u. a.: Electrochemical synthesis, characterization and thermal properties of niobium ethoxide. In: Journal of Central South University of Technology. 18, 2011, S. 73, Modul:Vorlage:Handle * library URIutil invalid.

