Okulärer Blutfluss
Okulärer Blutfluss (engl. ocular blood flow) beschreibt die Durchblutung des Auges, speziell die Blutversorgung der für die visuelle Wahrnehmung wichtigen anatomischen Strukturen Netzhaut, Aderhaut und Sehnerv. Der okuläre Blutfluss ist in der Medizin in zweierlei Hinsicht von Bedeutung: Die Netzhaut des Auges ist die einzige Stelle des menschlichen Körpers, an der Blutgefäße ohne invasive oder bildgebende Maßnahmen beobachtet und ihre Funktion quantifiziert bzw. gemessen werden kann. Zum anderen sind Charakteristika des okulären Blutflusses von diagnostischer Aussagekraft sowohl für bestimmte Augenerkrankungen wie Glaukom als auch für pathologische Veränderungen an anderen Organen wie zum Beispiel dem Herzen.
Anatomie
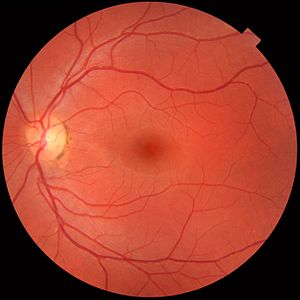
Die hinteren Augenabschnitte werden im Prinzip vom Blutkreislauf auf zwei Wegen versorgt. Die Aderhaut ist das am stärksten durchblutete Gewebe des Körpers. Von dieser Schicht – lateinischer Fachausdruck: Choroidea – aus werden die für die Sehwahrnehmung essentielle äußere Netzhautschicht versorgt, in der die lichtempfindlichen Fotorezeptoren, die Stäbchenzellen und Zapfenzellen der Retina liegen. Die andere Säule der Versorgung der Netzhaut ist die Zentralarterie (Arteria centralis retinae), die aus der Arteria ophthalmica entspringt und ebenso wie das abführende Blutgefäß, die Zentralvene (Vena centralis retinae) zusammen mit den Fasern des Sehnerven durch die Sehnervenscheibe (Papille) ins Auge ein- bzw. im Fall der Vene austritt. Diese beiden großen Gefäße bilden ein Netz, das den gesamten Augenhintergrund umfasst; sie verzweigen sich in immer kleinere Arteriolen und Venolen. Die Netzhaut ist das Gewebe im menschlichen Körper mit dem höchsten Sauerstoffbedarf – was deutlich macht, dass Störungen in der Blutversorgung mit Sehstörungen, im schlimmsten Fall mit irreversibler Schädigung des Sehorgans einhergehen.[1] Ein besonders drastisches derartiges Ereignis ist ein Verschluss der Zentralarterie, der meist zu Erblindung oder hochgradigem Sehverlust führt, aber auch krankhafte Veränderungen an den kleineren Verzweigungen der Gefäße können ausgeprägte und oft bleibende Einschränkungen des Sehvermögens verursachen. Vorübergehende Unterbrechungen einer adäquaten Blutzufuhr können zu einer Amaurosis fugax führen.[2]
Diagnostik
Die Gefäße der Netzhaut und je nach Untersuchungstechnik auch der Aderhaut sind für einen Arzt leicht einsehbar und morphologisch zu beurteilen. Eine direkte Beobachtung geschieht mit der Ophthalmoskopie. Der Vorgänger des Ophthalmoskops, der von Hermann von Helmholtz um 1850 erfundene Augenspiegel, ermöglichte erstmals einen direkten Blick auf die Netzhautgefäße und damit die Diagnose von okulären Gefäßkrankheiten. Mit heutigen Methoden lassen sich der okuläre Blutfluss messen und eventuelle Störungen nachweisen. Die Farbkodierte Doppler-Sonografie wird vor allem zur Beurteilung des Blutflusses in den retrobulbären Gefäßen eingesetzt, also den Arterien und Venen, die hinter dem Augapfel verlaufen. Eine andere Technologie, das Doppler-FD-OCT (Optische Kohärenztomografie) eignet sich zur Messung des gesamten Blutflusses in der Netzhaut. Eine quantitative Messung des Blutflusses in den Kapillaren der Netzhaut und der Aderhaut erlaubt auch die Laser-Doppler-Flowmetrie. Die Angiografie der Netzhautgefäße gibt zwar Hinweise auf die Qualität der okulären Perfusion und kann zum Beispiel Leckagen aus den Gefäßen nachweisen, doch erlaubt sie keine genaue Messung des Blutflusses.[3]
Eine besondere Rolle in der Beurteilung des okulären Blutflusses spielt die Retinale Gefäßanalyse. Während die statische Gefäßanalyse den Zustand der Netzhautgefäße dokumentiert, wird bei der dynamischen Gefäßanalyse mit einem optoelektrischen Flickerlicht eine Stimulation ausgeübt und die Änderung des Gefäßdurchmessers quantifiziert. Aus dem Verhalten der Netzhautgefäße wie zum Beispiel der Erweiterung des Gefäßdurchmessers als Reaktion auf die Lichtstimulation lassen sich Rückschlüsse auf die Gefäßsituation in anderen Körperregionen und Organen ziehen. Die Methode gibt Hinweise auf Gefäßschäden – zum Beispiel durch Alterungsprozesse oder Stoffwechselerkrankungen – bereits im Frühstadium.[4]
Abnormale Gefäßreaktionen bei der retinalen Gefäßanalyse sind unter anderen bei Herzerkrankungen und bei Patienten mit Risiken dafür (wie zum Beispiel Übergewicht) dokumentiert.[5][6]
Klinische Bedeutung
Störungen des okulären Blutflusses finden sich bei einigen der wichtigsten Augenerkrankungen wie Diabetische Retinopathie, altersabhängiger Makuladegeneration (AMD) und Glaukom. Vor allem bei einer häufigen Variante des Letzteren, dem Normaldruckglaukom ist eine generelle Durchblutungsproblematik mit einer sogenannten primären vaskulären Dysregulation, also mit Phasen einer unzureichenden Durchblutung aufgrund von Regulationsstörungen der Blutgefäße, als wesentlicher Risikofaktor identifiziert worden. Der Blutfluss im Auge ist beim Normaldruckglaukom stärker reduziert als beim Hochdruckglaukom (jener Variante der auch Grüner Star genannten Erkrankung, bei der ein erhöhter Augeninnendruck als wichtigste Krankheitsursache gilt).[7][8] Die Erforschung dieser vaskulären Komponente des Normaldruckglaukoms hat dazu geführt, einen Phänotyp zu identifizieren, der heute als Flammer-Syndrom bezeichnet wird. Es handelt sich dabei um Menschen mit einer generalisierten Fehlregulation der Blutgefäße, die in erhöhtem Maße anfällig sein können für bestimmte Beschwerdebilder und Erkrankungen, von kalten Händen und Füßen über Einschlafstörungen bis hin zu Tinnitus und Migräne. Die Untersuchung des okulären Blutflusses hat sich als wichtiger Schritt bei der Diagnosestellung etabliert.[9][10][11]
Die Bedeutung der Veränderungen des okulären Blutflusses aufgrund von Fehlregulationen der kleinen Gefäße als Prediktor von Herz-Kreislaufrisiken ist mit den gepoolten Daten zweier großer epidemiologischer Studien, der Beaver Dam Eye Study und der Blue Mountains Eye Study nachgewiesen und seither in weiteren Publikationen bestätigt worden.[12][13][14][15] Jüngst sind erstmals Störungen des okulären Blutflusses, nachgewiesen mit der retinalen Gefäßanalyse, als mit schweren Nierenschädigungen assoziiert beschrieben worden.[16] Noch im Anfangsstadium der Erforschung befindet sich ein möglicher Zusammenhang zwischen verzögerten Reaktionszeiten des okulären Blutflusses und der Alzheimer-Erkrankung.[17]
Internationale Forschung
Die Erforschung des okulären Blutflusses findet bislang überwiegend an spezialisierten Zentren statt; eine Vielzahl von wissenschaftlichen Publikationen dazu kommt vor allem aus Österreich und der Schweiz. Dort fand auch unweit von Luzern am Rigi im September 2019 der erste speziell dieser Thematik gewidmete internationale Kongress statt.[18]
Siehe auch
Einzelnachweise
- ↑ G. Tomita, D. Huang, C. O'Brien, K. H. Park, T. Nakazawa: Ocular Blood Flow and Visual Function. In: Biomed Res Int. 2015, Artikel 319254, doi:10.1155/2015/319254.
- ↑ A. Mirshahi, N. Feltgen, L. Hansen, L. O. Hattenbach: Gefäßverschlüsse der Netzhaut. Eine interdisziplinäre Herausforderung. In: Deutsches Ärzteblatt. 105(26), 2008, S. 474–479, doi:10.3238/arztebl.2008.0474.
- ↑ X. Luo, Y. M. Shen, M. N. Jiang, X. F. Lou, Y. Shen: Ocular Blood Flow Autoregulation Mechanisms and Methods. In: J Ophthalmol. 2015, Artikel 864871, doi:10.1155/2015/864871.
- ↑ Ronald D. Gerste: Spiegelbild der Mikrovaskulatur. In: Deutsches Ärzteblatt. 115(48), 30. November 2018, S. A2234–A2238.
- ↑ M. R. Nägele u. a.: Retinal microvascular dysfunction in heart failure. In: European Heart Journal. 39, 2018, S. 47–56, doi:10.1093/eurheartj/ehx565.
- ↑ H. Hanssen: Exercise-induced alerations of retinal vessel Diameters and cardiovascular risk reduction in obesity. In: Atherosclerosis. 216, 2011, S. 433–439, doi:10.1016/j.atherosclerosis.2011.02.009.
- ↑ K. Konieczka, S. Fränkl: Primäre vaskuläre Dysregulation und Glaukom (Primary Vascular Dysregulation and Glaucoma). In: Zeitschrift für praktische Augenheilkunde. 34, 2013, S. 207–215.
- ↑ N. P. Waldmann u. a.: The prognostic value of retinal vessel analysis in primary open-angle glaucoma. In: Acta Ophthalmologica. 94(6), 2016, S. e474–e480, doi:10.1111/aos.13014.
- ↑ Ronald D. Gerste: Augenleiden mit Tinnitus und kalten Extremitäten. Das Flammer-Syndrom beschreibt die Pathogenese einer Glaukomvariante, bei der vaskuläre Dysregulationen nicht nur im Auge dominieren. In: Deutsches Ärzteblatt. 21. Februar 2014, S. A308–A309.
- ↑ Maneli Mozaffarieh, Josef Flammer: Ocular blood flow and glaucomatous optic neuropathy. Springer, Berlin 2009, ISBN 978-3-540-69442-7.
- ↑ Katarzyna Konieczka, Robert Ritch, Carlo Enrico Traverso, Dong Myung Kim, Michael Scott Kook, Augusto Gallino, Olga Golubnitschaja, Carl Erb, Herbert A. Reitsamer, Teruyo Kida, Natalia Kurysheva, Ke Yao: Flammer syndrome. In: The EPMA Journal. 5, 2014, S. 11, doi:10.1186/1878-5085-5-11.
- ↑ J. J. Wang, G. Liew, R. Klein, E. Rochtchina, M. D. Knudtson, B. E. Klein, T. Y. Wong, G. Burlutsky, P. Mitchell: Retinal vessel diameter and cardiovascular mortality: pooled data analysis from two older populations. In: Eur Heart J. 28, 2007, S. 1984–1992, doi:10.1093/eurheartj/ehm221.
- ↑ J. Flammer, K. Konieczka, R. M. Bruno, A. Virdis, A. J. Flammer, S. Taddei: The eye and the heart. In: Eur Heart J. 34(17), Mai 2013, S. 1270–1278, doi:10.1093/eurheartj/eht023.
- ↑ M. P. Nägele, J. Barthelmes, V. Ludovici, S. Cantatore, A. von Eckardstein, F. Enseleit, T. F. Lüscher, F. Ruschitzka, I. Sudano, A. J. Flammer: Retinal microvascular dysfunction in heart failure. In: Eur Heart J. 39(1), Januar 2018, S. 47–56, doi:10.1093/eurheartj/ehx565.
- ↑ S. B. Seidelmann u. a.: Retinal Vessel Calibers in Predicting Long-Term Cardiovascular Outcomes. In: Circulation. 134, 2016, S. 1328–1338, doi:10.1161/CIRCULATIONAHA.116.023425.
- ↑ R. Günthner, H. Hanssen, C. Hauser u. a.: Impaired Retinal Vessel Dilation Predicts Mortality in End-Stage Renal Disease. In: Circ Res. April 2019, doi:10.1161/CIRCRESAHA.118.314318
- ↑ K. Kotliar, C. Hauser, M. Ortner u. a.: Altered neurovascular coupling as measured by optical imaging: a biomarker for Alzheimer’s disease. In: Scientific Reports. 7, S. 12906, doi:10.1038/s41598-017-13349-5.
- ↑ 1st Ocular Blood Flow Summit 2019, abgerufen am 16. Mai 2019.
Literatur
- Leopold Schmetterer, Jeffrey Kiel (Hrsg.): Ocular blood flow. Springer, Berlin 2012, ISBN 978-3-540-69468-7.
- D. Schmidl, L. Schmetterer, G. Garhöfer, A. Popa-Cherecheanu: Gender Differences in Ocular Blood Flow. In: Current Eye Research. 40(2), 2015, S. 201–212, doi:10.3109/02713683.2014.906625.
- G. Garhofer u. a.: Use of the retinal vessel analyzer in ocular blood flow research. In: Acta Ophthalmol. 88, 2010, S. 717–722, doi:10.1111/j.1755-3768.2009.01587.x.
- Katarzyna Konieczka, Konstantin Gugleta: Glaukom. Hans Huber, Bern 2015, ISBN 978-3-456-85146-4.