Carvon
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
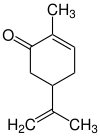
| |||||||||||||
| Vereinfachte Strukturformel ohne Stereochemie | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Carvon | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C10H14O | ||||||||||||
| Kurzbeschreibung | |||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 150,22 g·mol−1 | ||||||||||||
| Aggregatzustand | |||||||||||||
| Dichte |
etwa 0,965 g·cm−3[4] | ||||||||||||
| Siedepunkt |
etwa 230 °C[4] | ||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Carvon (Betonung auf der Endsilbe: Carvon) ist ein monocyclisches Monoterpen-Keton und Bestandteil von ätherischen Ölen.
Vertreter
Es gibt zwei enantiomere Carvone, das (S)-(+)-Carvon [auch als D-(+)-Carvon oder kurz (+)-Carvon bezeichnet] sowie das (R)-(−)-Carvon [auch als L-(−)-Carvon oder kurz (−)-Carvon bezeichnet].
| Enantiomere von Carvon | ||
| Name | (S)-(+)-Carvon | (R)-(−)-Carvon |
| Andere Namen | D-(+)-Carvon | L-(−)-Carvon |
| Strukturformel | 
|

|
| CAS-Nummer | 2244-16-8 | 6485-40-1 |
| 99-49-0 (Racemat) | ||
| EG-Nummer | 218-827-2 | 229-352-5 |
| 202-759-5 (Racemat) | ||
| ECHA-Infocard | 100.017.117 | 100.026.684 |
| 100.002.508 (Racemat) | ||
| PubChem | 16724 | 439570 |
| 7439 (Racemat) | ||
| FL-Nummer | 07.146 | 07.147 |
| 07.012 (Racemat) | ||
| Wikidata | Q27889969 | Q27089417 |
| Q416800 (Racemat) | ||
| Kurzbeschreibung | farbloses Öl, charakteristischer Geruch nach Kümmel |
farbloses Öl, charakteristischer Geruch nach Minze |
| Siedepunkt | 228–230 °C[2] | 230–231 °C[3] |
| Löslichkeit | schwer in Wasser (1300 mg/l bei 18 °C)[2] | praktisch unlöslich in Wasser (20 °C)[3] |
| LD50 | 3,71 ml·kg−1 (Ratte, peroral)[6] | 1640 mg·kg−1 (Ratte, peroral)[7] |
Vorkommen
In der Natur treten beide enantiomere Formen des Carvons auf. So ist (S)-(+)-Carvon enthalten in Kümmelöl (ca. 85 %),[8] Dill[9][8] und Mandarinenschalen. Das (R)-Enantiomer findet sich in den ätherischen Ölen von Krauseminze[10][8] und Kuromoji. Das Ingwergrasöl enthält beide enantiomeren Formen des Carvons (Racemat).[8]
Herstellung
(S)-(+)-Carvon gewinnt man durch Wasserdampfdestillation von Kümmel und Extraktion des Destillats.
Eigenschaften
Wie alle chiralen Duftstoffe weist auch Carvon unterschiedliche Geruchstypen seiner Enantiomere auf.[11][12] Das (S)-(+)-Carvon weist einen Kümmelgeruch auf, sein Spiegelbild (R)-(−)-Carvon riecht nach Krauseminze. Carvon wirkt keimhemmend.[13]
Analytik
Die qualitative und quantitative Bestimmung der Carvone gelingt nach adäquater Probenvorbereitung durch Kopplung der Kapillargaschromatographie und HPLC mit der Massenspektrometrie.[14]
Verwendung
Carvon wird als Ausgangsverbindung in der Naturstoffsynthese sowie bei der Herstellung von Likören, Kosmetik und Seife verwendet.[8]
Sicherheitshinweise
(R)-(−)-Carvon ist allergieauslösend.[15]
Weblinks
- Sicherheitsdatenblätter für (S)-(+)-Carvon:
- Datenblatt (S)-(+)-Carvon (PDF) bei Carl Roth, abgerufen am 8. Januar 2008.
- Datenblatt (S)-(+)-Carvon bei Merck, abgerufen am 8. Januar 2008.
- Sicherheitsdatenblätter für (R)-(−)-Carvon:
- Datenblatt (R)-(−)-Carvon (PDF) bei Carl Roth, abgerufen am 8. Januar 2008.
- Datenblatt (R)-(−)-Carvon bei Merck, abgerufen am 8. Januar 2008.
Einzelnachweise
- ↑ Eintrag zu Carvone bei Toronto Research Chemicals, abgerufen am 27. Januar 2022 (PDF).
- ↑ a b c d e f Eintrag zu (S)-2-Methyl-5-(1-methylethenyl)cyclohex-2-en-1-on in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Mai 2017. (JavaScript erforderlich)
- ↑ a b c d e f Eintrag zu (R)-2-Methyl-5-(1-methylethenyl)cyclohex-2-en-1-on in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Mai 2017. (JavaScript erforderlich)
- ↑ a b c Europäisches Arzneibuch 10.0. Deutscher Apotheker Verlag, 2020, ISBN 978-3-7692-7515-5, S. 730.
- ↑ Eintrag zu d-carvone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 17. Juni 2017. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag zu d-Carvone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 1. April 2017.
- ↑ Eintrag zu (-)-Carvone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 1. April 2017.
- ↑ a b c d e Eintrag zu Carvon. In: Römpp Online. Georg Thieme Verlag, abgerufen am 18. Dezember 2021.
- ↑ Birgit Faber, Kerstin Bangert, Armin Mosandl: GC-IRMS and enantioselective analysis in biochemical studies in dill (Anethum graveolens L.). In: Flavour and Fragrance Journal. Band 12, Nr. 5, September 1997, S. 305–309, doi:10.1002/(SICI)1099-1026(199709/10)12:5<305::AID-FFJ659>3.0.CO;2-7.
- ↑ Valtcho D. Zheljazkov, Charles L. Cantrell, Tess Astatkie, M. Wayne Ebelhar: Productivity, Oil Content, and Composition of Two Spearmint Species in Mississippi. In: Agronomy Journal. Band 102, Nr. 1, Januar 2010, S. 129–133, doi:10.2134/agronj2009.0258.
- ↑ G. F. Russel, J. I. Hills: Odor Differences between Enantiomeric Isomers. In: Science. 172, 1971, S. 1043–1044; doi:10.1126/science.172.3987.1043.
- ↑ L. Friedmann, J. G. Miller: Odor Incongruity and Chirality. In: Science. 172, 1971, S. 1044–1046; doi:10.1126/science.172.3987.1044.
- ↑ Kartoffeln (Solanum tuberosum) – Nahrung.
- ↑ C. Barba, R. M. Martínez, M. M. Calvo, G. Santa-María, M. Herraiz: Chiral analysis by online coupling of reversed-phase liquid chromatography to gas chromatography and mass spectrometry. In: Chirality. 24(5), Mai 2012, S. 420–426, PMID 22517436.
- ↑ A. T. Karlberg, K. Magnusson, U. Nilsson: Air oxidation of d-limonene (the citrus solvent) creates potent allergens. In: Contact Dermatitis. 26 (5), 1992, S. 332–340, PMID 1395597.


