Aluminiumchlorid
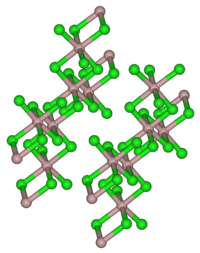
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Al3+ _ Cl− | ||||||||||||||||
| Kristallsystem |
monoklin | |||||||||||||||
| Raumgruppe |
C2/m (Nr. 12) | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Aluminiumchlorid | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Verhältnisformel | AlCl3 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 133,34 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,44 g·cm−3[3] | |||||||||||||||
| Sublimationspunkt | ||||||||||||||||
| Löslichkeit |
gut in Wasser (450 g·l−1 bei 20 °C, Zersetzung)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−704 kJ·mol−1[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Aluminiumchlorid ist eine anorganische chemische Verbindung; es ist das Chlorid des Aluminiums mit der Summenformel AlCl3.
Synthese
Wasserhaltiges Aluminiumchlorid (in rhombischen Kristallen auftretendes Hexahydrat AlCl3 · 6 H2O) entsteht durch Auflösen von Aluminium in Salzsäure:
Dieses Hexahydrat kann jedoch nicht entwässert werden, da es sich beim Erhitzen zu Aluminiumhydroxid bzw. Aluminiummetahydroxid und Chlorwasserstoffgas zersetzt:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{AlCl3.6H2O -> AlO(OH) + 3HCl + 4H2O}}
So muss die Herstellung von wasserfreiem Aluminiumchlorid durch Überleiten von Chlor über Kohlenstoff und Aluminiumoxid bei etwa 800 °C oder direkt aus den Elementen erfolgen:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{Al2O3 + 3C + 3Cl2 -> 2AlCl3 + 3CO}}
beziehungsweise:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{2Al + 3Cl2 -> 2AlCl3}}
Für die großtechnische Herstellung von Aluminiumchlorid werden aufgrund der hohen Aggressivität der beteiligten Reaktanten emaillierte Rührbehälter verwendet.
Eigenschaften
Aluminiumchlorid bildet farblose, hexagonale Kristalle (monokline Kristallstruktur, Raumgruppe C2/m (Raumgruppen-Nr. 12), a = 5,914 Å, b = 10,234 Å, c = 6,148 Å, β = 108,25°[7]). Es ist in vielen organischen Lösungsmitteln löslich. Das meist auf Grund von Verunreinigungen mit Eisenchloriden hellgelbe Pulver wirkt stark hygroskopisch. In feuchter Luft raucht es wegen teilweiser Hydrolyse zu Chlorwasserstoff und Aluminiumoxidchlorid. In Wasser löst es sich unter starker Erwärmung unter Bildung des Hexahydrats. In unpolaren Lösungsmitteln, flüssiger Phase sowie im Dampfzustand liegt Aluminiumchlorid als Dimer (Al2Cl6) vor, in dem das Aluminiumatom tetraedrisch koordiniert ist (analog zum Aluminiumbromid). Im festen Zustand liegt ein Ionengitter vor, in dem das Aluminiumion 6-fach durch Cl− koordiniert ist. Beim Schmelzen bricht das Ionengitter unter Bildung des Dimeren zusammen. Da dieses kovalent aufgebaut ist, leitet flüssiges Aluminiumchlorid den elektrischen Strom nur schlecht.[8]
Die Bindungsverhältnisse in Aluminium(III)-chlorid sind als Grenzfall zwischen kovalenter und ionischer Bindung einzuordnen, es hat eine Elektronegativitäts-Differenz ΔEN von 1,55 (nach Pauling). Damit sollte es sich eigentlich um eine polare Atombindung handeln.
Reaktionsverhalten
In stark exothermer Reaktion kommt Aluminiumchlorid in Wasser in Lösung, wobei eine Hydrolyse in Chloridionen und Hexaaquaaluminiumkomplexe erfolgt:
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{AlCl3 + 6H2O -> [Al(H2O)6]^{3+} {}+ 3Cl-}}
Diese Hexaaquaaluminiumionen wirken als schwache Säure (pKs = 4,97):[9]
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{[Al(H2O)6]^{3+} {}+ H2O -> [Al(H_{2}O)_{5}OH]^{2+} {}+ H3O+}}
Das Hydrat kann nicht durch Erhitzen zum wasserfreien Aluminiumchlorid entwässert werden, da unter Freisetzung von Wasser und Chlorwasserstoff das Aluminiumhydroxid bzw. das Aluminiumoxid entsteht.[10][11]
Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{[Al(H2O)6]Cl3 -> Al(OH)3 + 3HCl + 3H2O}}
- Fehler beim Parsen (MathML mit SVG- oder PNG-Rückgriff (empfohlen für moderne Browser und Barrierefreiheitswerkzeuge): Ungültige Antwort („Math extension cannot connect to Restbase.“) von Server „https://wikimedia.org/api/rest_v1/“:): {\displaystyle \ce{2[Al(H2O)6]Cl3 -> Al2O3 + 6HCl + 9H2O}}
Verwendung
Das Hexahydrat des Aluminiumchlorids findet auf Grund seiner stark adstringierenden Wirkung in der Textil- und Seifenindustrie Verwendung, wo es unter anderem der Herstellung von antiseptischen Mitteln oder Deodorants dient. Weiterhin wirkt es als starke Lewis-Säure sowie in der organischen Synthese (hier meist wasserfrei) als Katalysator bei Dehydrierungen, Polymerisationen und Friedel-Crafts-Reaktionen (Friedel-Crafts-Alkylierung, Friedel-Crafts-Acylierung). Außerdem wird es als Halogenüberträger und Kondensationsmittel verwendet.
Gegen leichte Entzündungen im Rachenraum werden Aluminiumchlorid- oder Aluminiumchlorat-haltige Lösungen zum Gurgeln angeboten. Es ist in Apotheken und Drogerien frei verkäuflich.
Aluminiumchlorid dient in der Dünnschichtchromatographie in Form eines Sprühreagenz zum Nachweis von Flavonoiden. Dazu werden 2,0 g Aluminiumchlorid-Hexahydrat in 100 mL einer 5%igen Lösung (V/V) von Eisessig in Methanol gelöst. Nach dem Aufsprühen dieser Lösung auf die DC-Platte erfolgt die Betrachtung im UV365-Licht. Dieses Reagenz wird unter der Bezeichnung Aluminiumchlorid-Reagenz R im Europäischen Arzneibuch (Ph. Eur.) gelistet.[12][13]
Sicherheitshinweise
Aluminiumchlorid wurde 2014 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Aluminiumchlorid waren die Besorgnisse bezüglich Exposition von Arbeitnehmern, hoher (aggregierter) Tonnage und hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Substanzen. Die Neubewertung läuft seit 2015 und wird von Frankreich durchgeführt. Um zu einer abschließenden Bewertung gelangen zu können, wurden weitere Informationen nachgefordert.[14]
Handelspräparate
Everdry (D), Gargarisma zum Gurgeln (D), Mallebrin (Ursprünglicher Wirkstoff Aluminiumchlorat[15]) (D)
AHC20 (CH), AHC30 (CH), Never-Sweat (D), Odaban (GB), Seven days (D), Yerka (D), Purax (D)
Siehe auch
Einzelnachweise
- ↑ Eintrag zu ALUMINUM CHLORIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- ↑ Eintrag zu Aluminiumchlorid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 11. November 2014.
- ↑ a b c d e f Datenblatt Aluminiumchlorid bei Merck, abgerufen am 4. Februar 2017.
- ↑ Eintrag zu Aluminiumchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- ↑ Eintrag zu Aluminium chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ PAETEC Formelsammlung Ausgabe 2003, S. 116.
- ↑ S. I. Troyanov: Crystal structures of titanium tetrachloroaluminate Ti(AlCl4)2 and refinement of AlCl3 crystal structure. In: Russian Journal of Inorganic Chemistry. 37, 1992, S. 266–272.
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente Wiley-VCH, 1990, ISBN 3-527-26169-9.
- ↑ A. F. Hollemann, N. Wiberg: Lehrbuch der anorganischen Chemie. 102. Auflage. De Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1158.
- ↑ G. Jander, E. Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie. 12. Auflage. S. Hirzel Verlag, Leipzig 1982, S. 275.
- ↑ A. F. Hollemann, N. Wiberg: Lehrbuch der anorganischen Chemie. 102. Auflage. De Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1152.
- ↑ E. Merck AG (Hrsg.): Anfärbereagenzien für Dünnschicht- und Papier-Chromatographie. Darmstadt 1965, S. 1.
- ↑ Europäisches Arzneibuch. 4.00 Auflage. Band 1. Deutscher Apotheker Verlag/Govi-Verlag – Pharmazeutischer Verlag GmbH, Stuttgart/Eschborn 2002, ISBN 3-7692-2947-9, S. 375.
- ↑ Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Aluminium chloride, abgerufen am 26. März 2019.
- ↑ Friedrich Mallebrein: Deutsch: Diese wissenschaftliche Veröffentlichung von Friedrich Mallebrein und C. Wasmer ist die Grundlage für die Erfindung des Medikaments Mallebrin. Auf der Suche nach Behandlungen für Tuberkulose entdecken Mallebrein und Wasmer interessante Wirkungen von Aluminiumchlorat gegen Beschwerden im Mund- und Rachenraum. Die Arbeit erschien in der Zeitschrift für Tuberkulose. Bd. 18, H. 3, 1912. 1912, abgerufen am 7. Dezember 2021.




