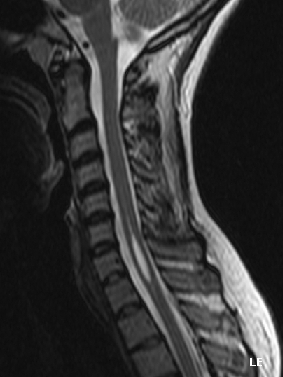
Syringomyelie
| Klassifikation nach ICD-10 | |
|---|---|
| G95.0 | Syringomyelie und Syringobulbie |
| ICD-10 online (WHO-Version 2019) | |
Die Syringomyelie (von altgriechisch
und
) ist eine röhrenförmige Höhlenbildung in der Grauen Substanz des Rückenmarkes. Synonym wird auch von Hydromyelie (von
) oder der Kombination beider Begriffe von Hydrosyringomyelie gesprochen.
Häufig ist das Hals- und Brustmark betroffen, bei Lokalisation in der Medulla oblongata wird sie Syringobulbie genannt.
Epidemiologie
Es ist eine seltene Erkrankung. Die Prävalenz lieg bei 8,4 pro 100.000 Einwohner,[1][2] wobei andere Studien zu abweichenden Prävalenzen kommen (bswp. 1,94 pro 100.000 Einwohner in Japan).[3] In Deutschland ist die Häufigkeit der Syringomyelie regional unterschiedlich: In Südwestdeutschland und in Österreich ist die Rückenmarkserkrankung häufiger zu finden.
Männer sind häufiger als Frauen betroffen. Typischerweise tritt die Erkrankung in der späten Pubertät oder im jungen Erwachsenenalter auf (zwischen dem 20. und 40. Lebensjahr).
Durch die vermehrte und verbesserte Bildgebung durch die Magnetresonanztomographie werden immer mehr Fälle von asymptomatischen Syringomyelien entdeckt. Eine epidemiologische Studie aus Japan zur Prävalenz der Syringomyelie kam zum Schluss, dass 22,7 % aller Syringomyelien keinerlei Symptome verursachen.[3]
Ursachen
Es existieren unterschiedliche Theorien zur Entstehung der Syringomyelie, wobei die Theorien nach der Form der Erkrankung auszudifferenzieren sind. Eine nicht-abschließende Liste von Entstehungstheorien ist nachfolgend aufgeführt:
- Hydrodynamische Theorie
- Saugeffekt-Theorie
- Piston-Theorie
- Vaskuläre Theorie
- Intramedulläre Puls-Druck-Theorie.[4]
Im Allgemeinen geht man heute davon aus, dass die Syringomyelie durch eine Blockade der Cerebrospinalflüssigkeit im Bereich des kraniozervikalen Übergangs und/oder der Wirbelsäule entsteht.
Die Häufigkeit der unterschiedlichen Ursachen wurde in diversen Studien untersucht, wobei in allen Fällen die Chiari-Malformation für mehr als 50 % der Fälle verantwortlich ist.
| Müller[5] | Brickel et al.[6] | |
|---|---|---|
| Chiari-Malformationen/
Wirbelsäulen- und |
56 % | 70,0 % |
| Zyste | 17 % | – |
| Trauma | 11 % | – |
| Tumor | 8 % | – |
| Unbekannt/Idiopathisch | 4 % | 16,1 % |
| Skoliose | 2 % | – |
| Andere | 2 % | – |
| Entzündung (z. B. Arachnoiditis) | 0 % | 13,9 % |
Weitere Ursachen, die in der Literatur diskutiert werden, sind das Tethered Cord,[7] Spinalkanalstenosen,[8] atlantoaxiale Instabilität,[9] und weitere Erkrankungen. Den meisten diskutierten Ursachen ist gemeinsam, dass sie für die Blockade des CSF-Flusses an einer oder mehreren Stellen im Bereich der Wirbelsäule oder des kraniozervikalen Übergangs verantwortlich sind.
Idiopathische Syringomyelie
Während heute weiterhin viele Informationsquellen im Internet und in der Fachliteratur von der Annahme ausgehen, dass die idiopathische Syringomyelie nicht ursächlich im Sinne einer Herbeiführung des Kollapses der Syrinx behandelbar ist, hat sich diese Einschätzung unter spezialisierten Radiologen und Neurochirurgen weitgehend geändert. Durch die Postulierung der o. g. CSF-Blockade als der Hauptursache für Syringomyelien wird der Anteil "echter" idiopathischer Fälle zunehmend geringer.[10] Wesentlich beteiligt an dem Rückgang der Fälle mit scheinbar unerklärlichen Ursachen ist die verbesserte Bildgebung mittels Magnetresonanztomographie. Speziell die Technik der pulsgetriggerten MRT-Phasenkontrastuntersuchungen (d. h. einer Bildgebung, die durch den Puls des Patienten ausgelöst wird und somit eine Darstellung des Liquor-Flusses möglich macht, sog. cardiac-gated cine steady-state free precession imaging magnet resonsance imaging) ermöglicht die Visualisierung von Blockaden im CSF-Fluss, die auf regulären MRT- oder CT-Aufnahmen nicht sichtbar werden. Oftmals handelt es sich dabei um Blockaden durch arachnoidale Zysten oder Gewebe.[11]
Untersuchungen mit Hilfe der neuen FLASH 2-Technologie[12] ermöglichen neuerdings auch Echtzeit-MRT-Aufnahmen des gesamten Körpers. Erste Untersuchungen bewiesen dabei, dass die Bewegung der Cerebrospinalflüssigkeit nicht mit dem Puls synchron verläuft, sondern von der Atmung abhängig ist. Somit ist der Weg für eine präzisere Bildgebung und die genaue Bestimmung von Blockaden im Schädel- und Wirbelsäulenbereich frei geworden. Jüngste Publikationen streichen hervor, dass die magnetrezonanztomographische Echtzeit-Bildgebung der Pathogenese von Syringomyelien entscheidend für das künftige Verständnis und die entsprechende zielgerichtetere Therapie sein wird.[13]
Formen
Angeboren
Der primären (angeborenen) Syrinx liegt oft eine so genannte Chiari-Malformation (Fehlbildung des zerebromedullären Überganges mit Kleinhirn-Tonsillen-Tiefstand) zugrunde. Die Verlagerung der Gehirnteile bewirkt eine chronische Liquorzirkulationsstörung, welche manchmal über einen Zeitraum von Jahren eine Rückenmarkshöhle ausbilden kann, die meistens im zervikalen oder thorakalen Rückenmark liegt.[14]
Angeboren kann es auch im Rahmen einer lumbalen Spina bifida oder eines seltenen kaudalen Regressionssyndroms zu einer Syrinx kommen.
Erworben
Eine Syrinx kann sich nach einer Verletzung, einem Tumor, einer Einblutung oder einer Entzündung der Hirnhäute (Meningitis) oder der Spinngewebshaut des Rückenmarkes (Arachnoiditis) entwickeln. Diese Form entwickelt sich mitunter auch noch Jahre nach einem Trauma oder nach multiplen, gar nicht erinnerlichen Mikrotraumata infolge einer Verklebung der Rückenmarkshäute mit folgender Liquorzirkulationsstörung. Bei dieser posttraumatischen Syringomyelie treten als Erstzeichen Schmerzen auf, welche sich von der Verletzungsstelle nach kopfwärts ausbreiten können.[15]
Symptome
Durch den Druck auf die umgebenden Nervenbahnen des Rückenmarks können diffuse Schmerzen (meist in Schultern oder Armen), Sensibilitätsstörungen oder Nervenlähmungen ausgelöst werden. Nach den ersten Symptomen kann es zu einer über Jahre bis Jahrzehnte dauernden langsamen Verschlechterung des Befindens kommen.
Die Größe einer Höhle korreliert nicht mit der Schwere der Erkrankung, vielmehr bestimmt die Lage der Syrinx und insbesondere die Druckwirkung auf das Nervengewebe die Symptomatik. Im fortgeschrittenen Stadium kann es durch eine lokale Blut-Minderversorgung zusätzlich zu einer Rückenmark-Schädigung kommen. Weiterhin kann es zu einer Einkammerung der Syrinx durch Wucherung von Gliazellen des Rückenmarks kommen.
Symptome sind unter anderem Muskelatrophie, Faszikulationen und Fibrillationen, besonders an den Armen mit Areflexie, Störungen der vegetativen Innervation mit vasomotorischen Symptomen, Ödemen, Hyperkeratosen, Horner-Syndrome, später, im Reflexbefund der Beine, Pyramidenbahnsymptome und spastische Lähmungen. Wegen des fehlenden Schmerzempfindens bei Temperaturreizen und spitzen Gegenständen können Verstümmelungen vorkommen, und da Gelenksüberlastungen nicht zeitig gespürt werden, auch vorzeitige Arthrosen, Knochenbrüche und Malum perforans. Bei begleitender Syringobulbie kommt es auch zu Nystagmus rotatorius mit Drehschwindel, Trigeminusstörungen, Lähmungen des Gaumensegels, der Stimmbänder oder einer Hemiatrophie der Zunge. Weitere häufige Symptome sind Verschlechterung des Sehvermögens, Skoliose, sexuelle Funktionsstörungen wie z. B. abnehmende Libido und Impotenz,[16] Depressionen, Krampfanfälle und Empfindungsstörungen ähnlich der Multiplen Sklerose.
Reicht die Syrinx bis in die unteren Hirnanteile, kann es zu Ausfallserscheinungen im Bereich der Hirnnerven kommen. Ebenfalls typisch für eine Höhle in dieser Lokalisation ist der Abbau von Muskelmasse (Muskelatrophie) im Bereich der Zunge. Auftreten können Empfindungsstörungen oder Schmerzen im Bereich des Gesichts. Diese Symptome treten oft einseitig auf und schreiten schnell fort.
Diagnose und Differenzialdiagnose
In ausgeprägten Fällen kann man im Röntgenbild eine Aufweitung des Spinalkanales sehen. Die angeborenen Formen können bereits mit einer spinalen Sonographie dargestellt werden.[17][18]
Üblicherweise erfolgt die Diagnose mittels Kernspintomographie (MRT) oder Computertomographie (CT). Ferner besteht die Möglichkeit einer CT-Myelographie mit Kontrastmittelgabe in den Liquor.
Eine eventuelle Lumbalpunktion mit Untersuchung des Nervenwassers dient dem Ausschluss bzw. genauerem Nachweis einer etwaigen Entzündung.
Die Differential-Diagnose umfasst unter anderen:
- Tumoren des Rückenmarkes
- Durchblutungsstörungen des Rückenmarkes
Therapie
Eine Heilung der Syringomyelie ist nicht möglich. Sie wird vor allem symptomatisch durch adäquate Schmerztherapie und Krankengymnastik behandelt. Durch die Schwierigkeit der Begrenzung von neuropathischen Schmerzen (hier Schmerzen durch Rückenmarksverletzungen oder -irritationen) kann sich die Schmerztherapie langwierig und schwierig darstellen, wobei oft eine Kombinationsbehandlung mit Neuroleptika und Antidepressiva durchgeführt wird. In schweren Fällen ist eine Schmerztherapie mit Opioiden (z. B. Buprenorphin, Fentanyl) erforderlich.
Operativ wird versucht, die Ursache (Verklebung, Vernarbung, Hautsegel u. a.) zu beheben oder, falls die Syringomyelie durch eine sogenannte Chiari-Malformation des Typs I/II bedingt ist, durch eine operative Verkleinerung des Kleinhirns oder eine Vergrößerung des Hinterhauptlochs eine Entlastung zu erreichen. Die Beschwerde-Symptomatik bildet sich aber meist nur unvollständig zurück. Bei der früher[19] häufigen Shunt-OP kann zusätzlich eine neue Syrinx als OP-Folge induziert werden, weswegen diese Operationsmethode mittlerweile meist nur noch in schwerwiegenden Fällen angewandt wird.
Prognose
Bei zirka einem Drittel der Patienten verläuft die Erkrankung sehr langsam oder kommt zu einem Stillstand. Bei einem Viertel, oft bei sekundär traumatisch erworbener Syrinx, findet sich eine zunehmende Verschlechterung, die auch nach operativer Therapie keine wesentliche Verlangsamung erfährt.
Für Betroffene
Für Betroffene gibt es einen international aktiven Verein, den Deutsche Syringomyelie und Chiari Malformation e.V. (DSCM e.V.), der von Betroffenen für Betroffene, Angehörige und sonst Interessierte (Ärzte, Physiotherapeuten etc.) gegründet wurde und von Fachärzten und Juristen unterstützend begleitet wird. Schirmherr ist Madjid Samii.
Syringomyelie beim Haushund
Eine Syringomyelie kommt gelegentlich auch beim Haushund vor. Besonders häufig betroffen ist der Cavalier King Charles Spaniel, aber auch bei anderen Zwerg- und kurzköpfigen Rassen kann eine Syringomyelie auftreten. Symptome sind Verhaltensweisen, die wie eine Reaktion auf Juckreiz aussehen, aber auch stärkere neurologische Symptome wie Ataxie, Schwäche, Krämpfe, dem Cluster-Kopfschmerz ähnliche Schmerzen,[20] Lähmungen oder Muskelschwund können auftreten.[21][22]
Die Behandlung kann chirurgisch durch eine Dekompression mit Durotomie erfolgen. Medikamentös kann eine Hemmung der Liquorproduktion mit Cimetidin, Furosemid oder Omeprazol, eine Schmerz- und Entzündungshemmung mit NSAID sowie eine Hemmung des Juckreizes mit Oclacitinib oder Gabapentin versucht werden.[21]
Literatur
- Klaus Poeck: Neurologie. 9. Auflage. Springer, 1996, ISBN 3-540-57942-7, S. 502 ff.
- Heinz-Walter Delank, Walter Gehlen: Neurologie. 12. Aufl., Thieme Verlag, 2010, S. 386 f., ISBN 3-13-129772-7.
- W. Pschyrembel, Klinisches Wörterbuch, Verlag Walter de Gruyter, 265. Auflage (2014) ISBN 3-11-018534-2.
- J. P. Kuhn, T. L. Slovis, J. O. Haller (Hrsg.): Caffey’s Pediatric Diagnostic Imaging. 10. Auflage, Mosby 2004. ISBN 0-323-01109-8.
Einzelnachweise
- ↑ orpha.net
- ↑ M. Brewis, D. C. Poskanzer, C. Rolland et al.: Neurological disease in an English city. Acta Neurologica Scand Suppl 24:1–89, 1966.
- ↑ a b Ken Sakushima, Satoshi Tsuboi, Ichiro Yabe, Kazutoshi Hida, Satoshi Terae: Nationwide survey on the epidemiology of syringomyelia in Japan. In: Journal of the Neurological Sciences. Band 313, Nr. 1, 15. Februar 2012, ISSN 0022-510X, S. 147–152, doi:10.1016/j.jns.2011.08.045, PMID 21943925 (Online [abgerufen am 14. August 2020]).
- ↑ Clare Rusbridge, Dan Greitz, Bermans J. Iskandar: Syringomyelia: Current Concepts in Pathogenesis, Diagnosis, and Treatment. In: Journal of Veterinary Internal Medicine. Band 20, Nr. 3, 2006, ISSN 1939-1676, S. 469–479, doi:10.1111/j.1939-1676.2006.tb02884.x (wiley.com [abgerufen am 14. August 2020]).
- ↑ Jennifer Müller vom Hagen: Differenzierung von Hydromyelie und Syringomyelie auf der Basis magnetresonanztomographischer, elektrophysiologischer und klinischer Untersuchungen. Hrsg.: Universität Tübingen. 2011 (online [abgerufen am 14. August 2020]).
- ↑ K. L. Brickell, N. E. Anderson, A. J. Charleston, J. K. A. Hope, A. P. L. Bok: Ethnic differences in syringomyelia in New Zealand. In: Journal of Neurology, Neurosurgery, and Psychiatry. Band 77, Nr. 8, August 2006, ISSN 0022-3050, S. 989–991, doi:10.1136/jnnp.2005.081240, PMID 16549414, PMC 2077633 (freier Volltext).
- ↑ Syringomyelia. In: NORD (National Organization for Rare Disorders). Abgerufen am 14. August 2020 (amerikanisches Englisch).
- ↑ Aaron F. Struck, Carrie M. Carr, Vinil Shah, John R. Hesselink, Victor M. Haughton: Cervical spinal canal narrowing in idiopathic syringomyelia. In: Neuroradiology. Band 58, Nr. 8, August 2016, ISSN 1432-1920, S. 771–775, doi:10.1007/s00234-016-1701-2, PMID 27194170.
- ↑ Abhidha Shah, Prashant Sathe, Manoj Patil, Atul Goel: Treatment of “idiopathic” syrinx by atlantoaxial fixation: Report of an experience with nine cases. In: Journal of Craniovertebral Junction & Spine. Band 8, Nr. 1, 2017, ISSN 0974-8237, S. 15–21, doi:10.4103/0974-8237.199878, PMID 28250632, PMC 5324354 (freier Volltext).
- ↑ SCOR Global: SCOR Global Life. Abgerufen am 14. August 2020 (englisch).
- ↑ Dynamic Visualization of Arachnoid Adhesions in Patients with Idiopathic Syringomyelia Using Cardiac-gated Cine Steady State Free Precession MRI at 1.5 T and 3T. Abgerufen am 14. August 2020.
- ↑ Echtzeit-Filme aus dem Körper. Abgerufen am 18. August 2020.
- ↑ Steffi Dreha-Kulaczewski, Mareen Konopka, Arun A. Joseph, Jost Kollmeier, Klaus-Dietmar Merboldt: Respiration and the watershed of spinal CSF flow in humans. In: Scientific Reports. Band 8, Nr. 1, 4. April 2018, ISSN 2045-2322, S. 1–7, doi:10.1038/s41598-018-23908-z.
- ↑ W. Schuster, D. Färber (Hrsg.): Kinderradiologie. Bildgebende Diagnostik. Springer 1996, ISBN 3-540-60224-0, S. 531
- ↑ B. Schurch, W. Wichmann, A. B. Rossier: Post-traumatic syringomyelia (cystic myelopathy): a prospective study of 449 patients with spinal cord injury. In: J. Neurol. Neurosurg. Psychiatr. 60, Nr. 1, Januar 1996, S. 61–7. doi:10.1136/jnnp.60.1.61. PMID 8558154. PMC 486191 (freier Volltext).
- ↑ DSCM: Symptome und Verlauf. (Nicht mehr online verfügbar.) Archiviert vom Original am 3. April 2012; abgerufen am 15. Februar 2020.
- ↑ L. H. Lowe, A. J. Johanek, C. W. Moore: Sonography of the Neonatal Spine: Part 2, Spinal Disorders, 2007, American Journal of Roentgenology 188, S. 739 ff, doi:10.2214/AJR.05.2160.
- ↑ M. Zieger, U. Dörr, R. D. Schulz: Pediatric spinal sonography. Part II: malformations and mass lesions. 1988 Pediatric Radiology 18, S. 105
- ↑ Vgl. auch V. Schmidden: Zur chirurgischen Behandlung der Syringomyelie. In: Zentralblatt für Chirurgie. Band 56, 1929, S. 2114 ff.
- ↑ M. Seijo-Martinez, M. Castro del Rio, C. Conde: Cluster-Like Headache: Association with Cervical Syringomyelia and Arnold-Chiari Malformation. doi:10.1111/j.1468-2982.2004.00597.x
- ↑ a b Stefanie Kruppke: Syringomyelie - neue Therapieoption am Horizont? In: veterinärspiegel Heft 2 2017, S. 53–55.
- ↑ Clare Rusbridge: Syringomelia