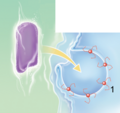
Vesicular stomatitis Indiana virus
| Indiana vesiculovirus | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

Vesicular stomatitis virus (VSV) | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
| ||||||||||||||||||||
| Taxonomische Merkmale | ||||||||||||||||||||
| ||||||||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||||||||
Indiana vesiculovirus
| ||||||||||||||||||||
| Kurzbezeichnung | ||||||||||||||||||||
| VSIV | ||||||||||||||||||||
| Links | ||||||||||||||||||||
|
Das Vesicular stomatitis Indiana virus (VSIV oder VSV-IN, offiziell Indiana vesiculovirus) ist eine aus der Familie der Rhabdoviridae stammende Virus-Spezies (Typusspezies) der Gattung Vesiculovirus. Damit ist es verwandt mit dem Tollwutvirus aus der Gattung Lyssavirus in derselben Virusfamilie. Es ist der Erreger der Stomatitis vesicularis, einer Infektionskrankheit der Huftiere. Auch beim Menschen kann es leichte grippale Symptome und selten Mundbläschen und Schwellung der Lymphknoten hervorrufen.[3] Das Wirtsspektrum umfasst Insekten, Rinder, Pferde und Schweine, weshalb es im Menschen eine Zoonose darstellt und Auswirkungen auf die Landwirtschaft aufweist. Die Symptome ähneln bei Rindern der (durch ein nicht näher verwandtes Virus hervorgerufenen) Maul- und Klauenseuche (MKS).
Vesicular-stomatitis-Viren
In der Gattung Vesiculovirus gibt es mehrere als Vesikuläres Stomatitis-Virus (englisch Vesicular stomatitis virus, VSV) bezeichnete Spezies:[4][5]
- Indiana vesiculovirus (Vesicular stomatitis Indiana virus, VSIV bzw. VSV-IN, Typusspezies)
- Alagoas vesiculovirus (Vesicular stomatitis Alagoas virus, VSAV bzw. VSV-AV)
- New Jersey vesiculovirus (Vesicular stomatitis New Jersey virus, VSNJV bzw. VSV-NJ)
Eigenschaften
Clathrin-vermittelter Eintritt in die Wirtszelle (VSV)
VSIV ist ein Arbovirus. Natürliche Infektionen mit VSIV durchlaufen zwei Phasen, eine lytische Phase in Säugern und eine persistente nicht-lytische Phase mit Insekten als Vektor.
VSIV ist ein typischer Vertreter der Gattung Vesiculovirus mit einzelsträngigem RNA-Genom in negativer Polarität. Das Genom codiert für fünf Proteine: Das Glykoprotein G, das Large-Protein (L, eine Polymerase), das Phosphoprotein (P), das Matrixprotein (M) und das Nukleoprotein (N).
Das Glykoprotein vermittelt die Adsorption und den Zelleintritt (Membranfusion) über ein Endosom, bevorzugt über Clathrin-Vesikel. Das Gen des VSIV L-Proteins macht die Hälfte des Genom aus und katalysiert die Replikation zusammen mit dem Phosphoprotein. Das Matrixprotein umhüllt das Ribonukleoprotein, bestehend aus dem viralen Genom, dem Nukleoprotein und den replikationsrelevanten Proteinen (L und P).[6]
Symptomatik
Die Symptome in Tieren umfassen Ulzerationen der Mucosa des Mauls, am Euter und um das Koronarband. Als mögliche systemische Symptome treten Kachexie, Lethargie und Pyrexie auf. Die Erkrankung kling meistens innerhalb zweier Wochen ab. Da keine medikamentöse Therapie existiert, basiert die Eindämmung auf Hygiene und Quarantäne.
Anwendungen
Das Glykoprotein des Virus wird häufig zur Pseudotypisierung in lentiviralen Vektoren eingesetzt.[7]
Die Brauchbarkeit des Virus als onkolytisches Virus zur Behandlung bösartiger Hirntumore sowie die zugrunde liegenden Mechanismen werden untersucht.[8][9][10][11]
Im Rahmen der Ebolafieber-Epidemie 2014 wurde von der Canadian National Microbiology Laboratory ein Impfstoff auf der Basis des Vesicular stomatitis virus mit Antigenen des Ebolavirus entwickelt und als VSV-EBOV ersten präklinischen Tests an Affen unterzogen. Phase I-Tests am Menschen sollen ab Herbst 2014 laufen.[12][13][14]
Über die Entwicklung eines weiteren möglichen Impfstoffs (gegen COVID-19, ausgelöst durch das Coronavirus SARS-CoV-2), wurde im August 2020 berichtet. Zu diesem Zweck wurde ein Hybridvirus, VSV-SARS-CoV-2 genannt, erzeugt, indem bei VSV das Virusgen für sein Oberflächenprotein gegen das Gen für das Spike-Protein von SARS-CoV-2 ausgetauscht wurde.[15][16]
Weblinks
- Vesiculovirus. In: ViralZone. Swiss Institute for Bioinformatics. Abgerufen am 3. Juni 2012.
- Vesicular Stomatitis Virus (Memento vom 12. Mai 2008 im Internet Archive) beim Lab-On-Site Project.
- wissenschaft.de: Mit Crispr/Cas gegen Viren (10. Oktober 2019)
Einzelnachweise
- ↑ a b ICTV: ICTV Taxonomy history: Akabane orthobunyavirus, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- ↑ ICTV Master Species List 2018b.v2. MSL #34, März 2019
- ↑ Vesicular Stomatitis Virus. In: Zoonoses. School of Veterinary Medicine, University Wisconsin, Madison WI. Archiviert vom Original am 9. Juni 2012. Abgerufen am 28. Januar 2019. (via WebArchiv)
- ↑ Vesicular Stomatitis, Center for Food Security & Public Health, Iowa State University, Januar 2016 (PDF).
- ↑ ICTV: Master Species List 2018a v1 MSL including all taxa updates since the 2017 release. Fall 2018 (MSL #33)
- ↑ Vesiculovirus. In: ViralZone. Swiss Institute for Bioinformatics. Abgerufen am 3. Juni 2012.
- ↑ J. Cronin, X. Y. Zhang, J. Reiser: Altering the Tropism of Lentiviral Vectors through Pseudotyping. In: Current Gene Therapy. 5, Nr. 4, 2005, S. 387–398. PMID 16101513. PMC 1368960 (freier Volltext).
- ↑ G. N. Barber: VSV-Tumor Selective Replication and Protein Translation. In: Oncogene. 24, Nr. 52, 2005, S. 7710–7719. doi:10.1038/sj.onc.1209042. PMID 16299531.
- ↑ T. P. Cripe, P. Y. Wang, P. Marcato, Y. Y. Mahller, P. W. K. Lee: Targeting Cancer-initiating Cells With Oncolytic Viruses. In: Molecular Therapy. 17, Nr. 10, 2009, S. 1677–1682. doi:10.1038/mt.2009.193. PMID 19672244. PMC 2835002 (freier Volltext).
- ↑ K. Özduman, G. Wollman, J. M. Piepmeier, A. N. van den Pol: Systemic Vesicular Stomatitis Virus Selectively Destroys Multifocal Glioma and Metastatic Carcinoma in Brain. (PDF) In: The Journal of Neuroscience. 28, Nr. 8, 2008, S. 1882–1893. doi:10.1523/JNEUROSCI.4905-07.2008. PMID 18287505.
- ↑ D. F. Stojdl, B. Lichty, S. Knowles, R. Marius, H. Atkins, N. Sonenberg, J. C. Bell: Exploiting Tumor-Specific Defects in the Interferon Pathway with a Previously Unknown Oncolytic Virus. In: Nature Medicine. 6, Nr. 7, 2000, S. 782–789. doi:10.1038/77558. PMID 10888934.
- ↑ Philipp Graf: Die Anti-Ebola-Offensive. In: Transkript. Heft 9, 2014, S. 18–19.
- ↑ Canada offers experimental Ebola vaccine VSV-EBOV to West Africa. CBC News. 12. August 2014. Abgerufen am 11. Oktober 2014.
- ↑ Canada's experimental Ebola vaccine: How does it work?. CTV News. 13. August 2014. Abgerufen am 11. Oktober 2014.
- ↑ SciTechDaily: Researchers Created a Virus That Mimics SARS-CoV-2, the COVID-19 Coronavirus – Here’s Why. Quelle: Washington University School of Medicine. 19. August 2020
- ↑ James Brett Case, Paul W. Rothlauf, Rita E. Chen, Zhuoming Liu, Haiyan Zhao, Arthur S. Kim, Louis-Marie Bloyet, Qiru Zeng, Stephen Tahan, Lindsay Droit, Ma. Xenia G. Ilagan, Michael A. Tartell, Gaya Amarasinghe, Jeffrey P. Henderson, Shane Miersch, Mart Ustav, Sachdev Sidhu, Herbert W. Virgin, David Wang, Siyuan Ding, Davide Corti, Elitza S. Theel, Daved H. Fremont, Michael S. Diamond and Sean P. J. Whelan: Neutralizing Antibody and Soluble ACE2 Inhibition of a Replication-Competent VSV-SARS-CoV-2 and a Clinical Isolate of SARS-CoV-2, in: Cell Host and Microbe, 3. Juli 2020 (online), doi:10.1016/j.chom.2020.06.021