4-Pyridon
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||
| Allgemeines | |||||||||||||
| Name | 4-Pyridon | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C5H5NO | ||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 95,10 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
230–235 °C (16 hPa)[2] | ||||||||||||
| Löslichkeit |
löslich in Wasser[2] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
4-Pyridon ist eine organische Verbindung mit der Summenformel C5H5NO. Sie gehört zur Gruppe der Pyridone.
Darstellung
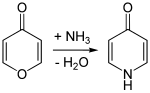
Analog dem isomeren 2-Pyridon kann 4-Pyridon durch Umsetzung von 4-Pyron mit Ammoniak erhalten werden.[1]
Eigenschaften
Die Ketoform 4-Pyridon liegt im chemischen Gleichgewicht mit der tautomeren Hydroxoform 4-Hydroxypyridin[4]. In Lösung liegt das Gleichgewicht fast vollständig auf der Seite des Ketons.[1] Die Hydroxoform stellt nur in stark verdünnter Lösung sowie in sehr unpolaren Lösungsmitteln einen signifikanten Anteil im Gleichgewicht dar. In der Gasphase hingegen ist die Hydroxoform die dominante Spezies.[5]
Das Reaktionsverhalten von 4-Pyridon wird durch die Ketoform bestimmt, weshalb die Bezeichnung 4-Pyridinol vermieden werden sollte, da sie eine Reaktivität ähnlich dem Phenol impliziert, die jedoch nicht auftritt. In Lösung weist 4-Pyridon keine klassisch aromatischen Eigenschaften auf. So besitzt das isomere 3-Hydroxypyridin einen pyridintypischen pKs-Wert, während 4-Pyridon eine deutlich geringere Basizität aufweist und amidähnlich am Sauerstoff protoniert wird.[5]
Mit Eisen(III)-chlorid bildet 4-Pyridon gelbgefärbte Komplexe.[1]
Vorkommen und Verwendung
4-Pyridon in freier Form besitzt keine natürlichen Vorkommen, jedoch tritt das Grundgerüst als struktureller Baustein in Pyridosin, einem Hydrolyseprodukt von Milch auf. Ferner tritt es im Naturstoff Mimopudin und der nicht-biogenen Aminosäure Mimosin auf.[1]
Die Verbindung dient als Grundstoff zur Synthese von 4-Chlorpyridin und 3-Hydroxy-4-pyridonen. Letztere werden als Aluminium- und Eisen-bindende Medikamente eingesetzt.[1]
Einzelnachweise
- ↑ a b c d e f Eintrag zu Pyridinole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- ↑ a b c Datenblatt 4-Pyridon bei AlfaAesar, abgerufen am 6. März 2010 (PDF) (JavaScript erforderlich).
- ↑ a b Datenblatt 4-Hydroxypyridine bei Sigma-Aldrich, abgerufen am 22. Oktober 2016 (PDF).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4-Hydroxypyridin: CAS-Nummer: 626-64-2, EG-Nummer: 210-958-3, ECHA-InfoCard: 100.009.963, Wikidata: Q24730939.
- ↑ a b J. A. Joules, K. Mills: Heterocyclic Chemistry 2000, 4. Auflage, Blackwell Science, Oxford, S. 88–91; ISBN 0-632-05453-0.