Palmitinsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
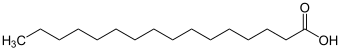
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Palmitinsäure | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C16H32O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose, kristalline Plättchen[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 256,43 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
0,8577 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
351 °C[4] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,4335[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
nicht vergeben[4] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Palmitinsäure (Hexadecansäure) ist eine gesättigte organische Säure und wird zu den Fettsäuren (= höhere Carbonsäuren) gezählt. Palmitate (systematisch auch Hexadecanoate) sind die Salze und Ester der Palmitinsäure. Palmitinsäure ist bei Zimmertemperatur ein farbloser Feststoff.
Palmitat ist in vielen Lebewesen ein Haupt-Zwischenprodukt des Stoffwechsels, aus dem alle anderen Fettsäuren für den Aufbau von Fettreserven in Form von Glyceriden hergestellt werden. Die Biosynthese von Palmitat erfolgt in der Lipogenese aus kleinen Molekülvorstufen in einem sich wiederholenden Prozess, in dem mit jedem Schritt zwei Kohlenstoffmoleküle an die Molekülkette gehängt werden.
Der Name Palmitinsäure stammt aus der ersten Gewinnung durch Verseifen von Palmöl durch Edmond Frémy (um 1840).[2]
Vorkommen

Der Palmitinsäurerest ist der in vielen pflanzlichen und tierischen Fetten und fetten Ölen als Glycerinester am häufigsten vorkommende gesättigte Fettsäurerest:
| Produkt | Gehalt an Palmitinsäure[2] |
|---|---|
| Stillingiaöl | 60–70 % |
| Palmöl | 41–46 % |
| Butterfett | 24–32 % |
| Schweineschmalz | 24–30 % |
| Kakaobutter | 23–30 % |
| Rindertalg | 23–29 % |
| Baumwollsaatöl | 21–27 % |
| Avocadoöl | 10–26 % |
Entgegen weitverbreiteter Anschauung enthalten natürliche Fette und Öle keine freie Palmitinsäure, sondern deren Glycerinester. Der Samen von Crotalaria ochroleuca enthält ca. 50 % freie Palmitinsäure.[6]
Physikalische Eigenschaften
Der Flammpunkt liegt bei >160 °C, die Zündtemperatur bei 240 °C und die untere Explosionsgrenze bei 0,42 Vol.-%.[4]
Analytik
Die sichere qualitative und quantitative Bestimmung der Palmitinsäure in den verschiedensten Untersuchungsmaterialien gelingt nach adäquater Probenvorbereitung und Umesterung zum Methylester durch Kopplung der Kapillargaschromatographie mit der Massenspektrometrie.[7][8][9]
Gesundheitliche Risiken
Ermöglicht "vorhandenen" Tumoren Metastasten zu bilden, und zu streuen.[10]
Verwendung
Palmitate werden häufig in Kosmetika verwendet.
Das Aluminiumsalz der Palmitinsäure bildet, zusammen mit dem Aluminiumsalz der Naphthensäure, das Verdickungsmittel der Brandwaffe Napalm, dessen Name sich aus den Anfangssilben der Säuren zusammensetzt (Naphthensäure, Palmitinsäure).
Eine alkoholische Kaliumpalmitatlösung (standardisierte Schmierseife) dient zur Bestimmung der Gesamthärte in Wasser.
Weblinks
Einzelnachweise
- ↑ Eintrag zu PALMITIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2019.
- ↑ a b c d e f g Eintrag zu Palmitinsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 20. Juni 2014.
- ↑ a b David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 96. Auflage. CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-294.
- ↑ a b c d e f Eintrag zu CAS-Nr. 57-10-3 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Dezember 2019. (JavaScript erforderlich)
- ↑ C. D. Cappa, E. R. Lovejoy, A. R. Ravishankara: Evaporation Rates and Vapor Pressures of the Even-Numbered C8–C18 Monocarboxylic Acids. In: J. Phys. Chem. A 112, 2008, S. 3959–3964. doi:10.1021/jp710586m
- ↑ H. J. Bestmann, M. Pietschmann, K. Steinmeier, O. Vostrowsky: Flüchtige Inhaltsstoffe von Crotalaria ochroleuca und deren Wirkung auf Schadinsekten / Volatile Constituents from Crotalaria ochroleuca and Their Effect on Pest Insects. In: Zeitschrift für Naturforschung C. 46, 1991, S. 579–584 (PDF, freier Volltext).
- ↑ D. M. Cassidy, D. A. Pratt, R. Taylor, K. G. Alberti, M. F. Laker: Capillary column gas chromatography-mass spectrometry for the determination of the fatty acid composition of human adipose tissue. In: J Chromatogr. 491(1), 30. Jun 1989, S. 1–13. PMID 2793965
- ↑ N. N. Ahmad Nizar, J. M. Nazrim Marikkar, D. M. Hashim: Differentiation of lard, chicken fat, beef fat and mutton fat by GCMS and EA-IRMS techniques. In: J Oleo Sci. 62(7), 2013, S. 459–464. PMID 23823911
- ↑ X. Dong, Y. Gao, M. Zeng, M. Liu, W. Li, Q. Liu, B. Wang: Analysis of meibum by gas chromatography-mass spectrometry. In: Zhonghua Yan Ke Za Zhi. 51(9), Sep 2015, S. 668–672. (chinesisch) PMID 26693651
- ↑ Gloria Pascual, Diana Domínguez, Marc Elosúa-Bayes, Felipe Beckedorff, Carmelo Laudanna: Dietary palmitic acid promotes a prometastatic memory via Schwann cells. In: Nature. Band 599, Nr. 7885, November 2021, ISSN 1476-4687, S. 485–490, doi:10.1038/s41586-021-04075-0 (nature.com [abgerufen am 20. November 2021]).