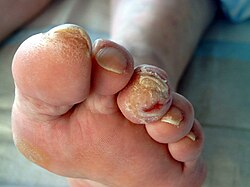
Diabetisches Fußsyndrom
| Klassifikation nach ICD-10-GM | |
|---|---|
| E14.74+ | Nicht näher bezeichneter Diabetes mellitus mit diabetischem Fußsyndrom, nicht als entgleist bezeichnet |
| E14.75+ | Nicht näher bezeichneter Diabetes mellitus mit diabetischem Fußsyndrom, als entgleist bezeichnet |
| G63.2* | Diabetische Polyneuropathie |
| I79.2* | Periphere Angiopathie bei anderenorts klassifizierten Krankheiten |
| ICD-10 online (GM-Version 2021) | |
Das Diabetische Fußsyndrom (DFS), umgangssprachlich auch „diabetischer Fuß“ genannt, ist ein Syndrom krankhafter Veränderungen auf der Grundlage einer schmerzlosen sensorischen Neuropathie und/oder einer peripheren arteriellen Verschlusskrankheit (PAVK) bei Diabetes mellitus. Es findet sich am häufigsten bei Patienten mit Diabetes mellitus Typ 2 und ist mit einem hohen Risiko für schlecht heilende Wunden am Fuß verbunden.
Epidemiologie
Etwa 15 % der Diabetiker entwickeln im Laufe ihres Lebens in Folge ihrer Erkrankung schmerzlose, schlecht heilende Wunden an den Füßen. Dieses Risiko betrifft eine Million Menschen mit Diabetes in Deutschland.[1] Schätzungen gehen davon aus, dass in Deutschland derzeit 250.000 Diabetiker eine Fußwunde haben.[2] Pro Jahr entsteht bei 4 % der Diabetiker eine neue Wunde, bei 0,1 % kommt es durch den Zusammenbruch des Fußgewölbes zu einem Charcot-Fuß.[1]
Ursache
Im Rahmen eines unzureichend kontrollierten Diabetes mellitus mit dauerhaft überhöhtem Blutzuckerspiegel (Hyperglykämie) kommt es auf bisher nicht geklärte Weise zu chronischen Schädigungen insbesondere an den Augen, den Nieren und den Nerven, wobei für den diabetischen Fuß zwei Schädigungen entscheidend sind:
- Diabetische Neuropathie: im Rahmen der diabetesbedingten Nervenschädigung (Polyneuropathie) ist die Schmerzempfindung oft stark reduziert oder fehlt ganz[3], so dass auch große und tiefe Wunden nicht wahrgenommen werden. Die Wunden entstehen oft – unbemerkt – bei banalen Unfällen, nach nicht sachgemäßer Fußpflege, bei Steinchen im Schuh, bei zu starker Belastung besonders bei Fußfehlstellungen oder bereits durch Anstoßen der Zehenspitzen im Schuh oder gegen Kanten. Um die Schutzbedürftigkeit des Patienten eindeutig festlegen zu können, ist die Früherkennung einer Neuropathie von großer klinischer Bedeutung; dazu werden Rydel-Seiffer-Stimmgabel, Monofilament-, Pinprick-Test, Temperaturdiskrimination, Muskeleigenreflex- und weitere Tests eingesetzt.[4] Der Fuß hat oftmals ein charakteristisches Aussehen:[5]
- Haut ist rosig, warm und trocken
- Taubheitsgefühl, Brennen, Kribbeln in den Zehen und den Füßen.
- Das Gefühl, auf Watte zu laufen sowie das Gefühl, kalte Füße zu haben, obwohl diese warm sind.
- Schmerz bei ruhenden Füßen, vor allem nachts und Schmerzlinderung durch Umhergehen
- Füße neigen zu Verhornung und zu Nagelpilz.
- Verminderung oder Verlust von Vibrations-, Temperatur- und Schmerzempfinden (Wahrnehmungsschwellen sind erhöht!)
- Diabetische Angiopathie: durch Schädigung großer und kleiner Gefäße und der Regulation des Gefäßtonus entstehen Durchblutungsstörungen der Extremitäten. Auch hierbei findet sich in der reinen Form ein charakteristisches Aussehen (wenngleich oft Mischbilder vorliegen):[5]
- kalte Füße, verdickte Nägel
- Dünne, pergamentartige, bläulich blasse Haut, besonders am Vorfuß
- Druckstellen (rötl. Hautflecken, die sich nicht wegstreichen lassen)
- Wadenschmerzen oder -krämpfe beim Gehen – Linderung durch Stehenbleiben, umgangssprachlich auch Schaufensterkrankheit (lat.: Claudicatio intermittens) genannt.
Zum Großteil wird das Diabetische Fußsyndrom (in 40 bis 60 %) allein durch eine Polyneuropathie ausgelöst.[6] Wunden, die infolge einer Polyneuropathie entstehen, treten insbesondere an Stellen auf, die besonderem Druck ausgesetzt sind, meist am Fußballen oder an der Fußunterseite. 15 % der Fälle sind auf eine Periphere arterielle Verschlusskrankheit (pAVK) zurückzuführen.[6] Solche Wunden befinden sich oft an den Zehen und Zehenspitzen, wo die Durchblutungssituation am schlechtesten ist. Zu etwa einem Drittel ist ein Zusammenwirken von Neuropathie und pAVK die Ursache für eine Wundentstehung.[6] Kommen beide Risikofaktoren zusammen, ist das Ulkus-Risiko deutlich höher und die Heilungschancen deutlich niedriger.
Eine typische rein neuropathische Wunde am Fuß ist das Malum perforans. Ohne adäquate Behandlung können die Hautgeschwüre (Ulzerationen) immer tiefer in den Fuß hineinreichen und auch mit MRSA-Keimen besiedelt werden, die eine normale Wundversorgung und -heilung verhindern können. Darüber hinaus besteht die Gefahr einer Infektion und einer Infektausbreitung über Lymphgefäße (Lymphangitis) oder die Blutbahn (Septikämie) bis hin zur Sepsis (Blutvergiftung), die mit einer hohen Sterblichkeit verbunden ist.
Charcot-Fuß
| Klassifikation nach ICD-10 | |
|---|---|
| E14.6+[7] | Nicht näher bezeichneter Diabetes mellitus mit sonstigen näher bezeichneten Komplikationen |
| M14.6*[7] | Neuropathische Arthropathie |
| ICD-10 online (WHO-Version 2019) | |
Eine weitere Ursache von Zerstörungen von Knochen und Gelenken am Fuß ist die diabetisch-neuropathische Osteoarthropathie (DNOAP, auch Charcot-Fuß genannt). Sie entsteht im Rahmen der Polyneuropathie. Durch die Fehlstellung und die Überlastung, die durch die Polyneuropathie nicht schmerzhaft ist, sowie eine häufig vorliegende Osteopenie kann es zu einem Ermüdungsbruch einzelner Fußknochen kommen. Da die Schmerzschwelle extrem erhöht und somit kein Schmerzempfinden mehr vorhanden ist, belasten viele Betroffene wochenlang den gebrochenen Fuß weiter. Der Fuß wird warm, geschwollen und rot im Vergleich zur Gegenseite. Der Schmerz fällt dabei geringer als erwartet aus oder kann sogar trotz erheblicher Knochenbrüche ganz ausbleiben. In diesem Stadium zeigt die Magnetresonanztomografie (MRT) ein Knochenmarködem, das durch sofortige strikte Entlastungsbehandlung günstigstenfalls völlig ausgeheilt werden kann. Zum Arzt führt leider oft erst die auffällige Deformierung des Fußes im Spätstadium des Krankheitsbildes. Die Diagnostik baut dann auf einer Röntgenuntersuchung auf und umfasst die sogenannten „5 D der radiologischen Manifestation des DNOAP“.[8]
- Distension der Gelenke
- Dislokation von Knochen und Gelenken
- Debris des Knochens
- Desorganisation der Knochen und Gelenke
- Dichteerhöhung in den Knochen
Als Therapie der Osteoarthropathie erfolgt zunächst die komplette Entlastung (Bettruhe), dann die teilweise Entlastung z. B. in Gipsverbänden, später müssen spezielle orthopädische Maßschuhe getragen werden.[9] Gegebenenfalls sind orthopädische Eingriffe notwendig, um die Fehlstellung operativ zu korrigieren und lokale Überlastungen auszugleichen.
Diagnostik
Die Diagnostik besteht zum einen in der Befundung der diabetischen Fußwunde, kann und sollte zum anderen aber weiter gefasst werden und die Ursachen mit erfassen. Um beides zu beurteilen haben sich neben vielen anderen Klassifikationen zwei im deutschsprachigen Raum etabliert:
Wagner-Armstrong-Klassifikation der diabetischen Fußwunde
Die Tiefe einer Wunde, die am Fuß infolge des diabetischen Fußsyndroms entstanden ist, wird anhand der Gradeinteilung nach Wagner erfasst. Hierbei wird lediglich die Wunde und nicht die Fußdeformitäten beurteilt, also nur ein Aspekt des Syndroms bewertet, was als Problematik der Wagner-Einteilung angesehen wird. Dennoch ist diese Einteilung weit verbreitet.[10] In Kombination mit dem University of Texas Diabetic Foot Classification System, kurz „Armstrong-Stadieneinteilung“ (links: A bis D), werden die Wagner-Grade (oben: 0 bis 5) zu den Faktoren Ischämie und Infektion in Bezug gesetzt, wodurch die im deutschsprachigen Raum gebräuchliche Wagner-Armstrong-Klassifikation entsteht.[11]
| 0 | 1 | 2 | 3 | 4 | 5 | |
|---|---|---|---|---|---|---|
| A | keine Läsion liegt vor | Eine oberflächliche Wunde besteht | Die Wunde reicht zur Sehne und/oder Gelenkkapsel | Knochen und/oder Gelenke sind geschädigt | teilweise Nekrose des Fußes | Nekrose am gesamten Fuß |
| B | Mit Infektion[12] | Mit Infektion | Mit Infektion | Mit Infektion | Mit Infektion | Mit Infektion |
| C | Mit Ischämie[13] | Mit Ischämie | Mit Ischämie | Mit Ischämie | Mit Ischämie | Mit Ischämie |
| D | Mit Infektion und Ischämie[14][15] | Mit Infektion und Ischämie | Mit Infektion und Ischämie | Mit Infektion und Ischämie | Mit Infektion und Ischämie | Mit Infektion und Ischämie |
angelehnt an: D. Hochlenert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie. (2014) und K. Hodeck, A. Bahrmann (Hrsg.): Pflegewissen Diabetes. (2014)
PEDIS-Klassifikation
International ist die von der International Working Group on the Diabetic Foot (IWGDF) erarbeitete PEDIS-Klassifikation verbreitet.[10] Diese Einteilung wurde 2004 von dem Maastrichter Internisten Nicolaas Schaper vorgestellt.[16] Das Akronym PEDIS (lat: Genetiv Singular zu pes=Fuß) setzt sich aus den Anfangsbuchstaben der fünf hierbei betrachteten Faktoren zusammen:
- Perfusion: Die Durchblutungssituation in der betroffenen Extremität wird in drei Schweregrade unterteilt.
- Extent: Die Wundgröße wird im Anschluss an ein Debridement erfasst und in cm² angegeben.
- Depth: Die Wundtiefe und -ausdehnung orientiert sich am geschädigten Körpergewebe und umfasst drei Grade
- Infektion: Das Vorliegen und die Ausprägung einer Infektion wird in vier Graden erfasst.
- Sensation: Das Gefühl für den Fuß wird in zwei Grade eingeteilt, hierbei wird erfasst, ob der Patient seinen Fuß uneingeschränkt (Grad 1) oder eingeschränkt (Grad 2) wahrnimmt.
Leibesinselschwund
Die reduzierte Schmerzwahrnehmung des Betroffenen in den unteren Extremitäten ist kennzeichnend für das Diabetische Fußsyndrom. Durch Unachtsamkeit gegenüber dem Zustand der eigenen Füße können sich kleine Verletzungen unbemerkt zu erheblichen Schädigungen entwickeln. Die manchmal ungewöhnlich wirkende diesbezügliche Achtlosigkeit Betroffener könnte durch den sogenannten Leibesinselschwund erklärt werden.[17] Das Konzept der Leibesinseln beschreibt unseren Körper, der nicht als Ganzes, sondern nur in seinen einzelnen Regionen wahrgenommen werden kann, als Ansammlung bsp. gastraler, oraler oder analer „Inseln“. Die Systematik der Leibesinseln wurde nach dem Ersten Weltkrieg an Patienten erforscht, die in Folge einer Kriegsverletzung amputiert werden mussten, ihre verlorenen Glieder aber weiterhin wahrnahmen. Hieraus leitete sich die für dieses Konzept getroffene Unterscheidung zwischen vorhandenem Körper und wahrgenommenem Leib ab. Als Folge ihrer diabetischen Polyneuropathie beim diabetischen Fußsyndrom spüren Patienten ihre unteren Gliedmaßen weniger oder gar nicht mehr, was in ihrer Wahrnehmung zu einem Verschwinden der betroffenen Regionen führt: zum Leibesinselschwund.[18] Der betroffene Fuß wird nicht mehr zum eigenen Körper gezählt, sondern als Teil der Umgebung und als „Problem des Arztes“ wahrgenommen.
Vorbeugung
Vorbeugende Maßnahmen zur Vermeidung des Diabetischen Fußsyndroms betreffen alle Menschen mit Diabetes und mit eingeschränkter Empfindung oder Durchblutungsstörungen.
Hautpflege
Allgemein sollten Menschen mit einer Diabeteserkrankung Wert auf eine gute Hautpflege legen. Regelmäßige Hautpflegemaßnahmen dienen auch der Beobachtung der Hautareale, bei denen aufgrund des verminderten Schmerzempfindens infolge des Diabetes, unbemerkt Schädigungen entstehen können. Zur Nagel- und Schwielenpflege dürfen keine scharfen Gegenstände verwendet werden (auch nicht von Fußpflegern), stattdessen Nagelfeilen und Bimssteine. Geeignete Hautpflegeprodukte enthalten Feuchthaltefaktoren wie Glycerin, Milchsäure und Urea. Zum Einsatz kommen Cremes oder Pflegeschäume auf Wasser-in-Öl Basis. Um einem unbeobachteten Pilzbefall oder Mazeration vorzubeugen, werden diese Produkte nicht in den Zehenzwischenräumen aufgetragen, sondern auf Fußsohle und Fußrücken. Fußpilz soll konsequent behandelt werden und Zehenzwischenräume nach dem Baden sorgfältig getrocknet werden. Die Schuhe müssen ausreichend weit und weich sein und die Füße täglich auf Verletzungen geprüft werden, z. B. mit einem Rasierspiegel.
Weitere Maßnahmen
Als Maßnahmen zur Vorbeugung des diabetischen Fußulkus werden empfohlen
- Täglich die Füße genau ansehen und auf Verletzungen sowie Druckstellen überprüfen. Auf Schwellungen prüfen, indem mit der Hand über den Fuß gestrichen wird, auch nach dem Tragen neuer Schuhe oder nach langen Spaziergängen/Wanderungen Füße überprüfen.
- Täglich mit lauwarmem Wasser waschen. Nicht länger als drei Minuten, gut trocknen, besonders in den Zehenzwischenräumen.
- Haut gut eincremen mit harnstoffhaltigen Cremes, um Risse (Rhagade/Schrunde) zu vermeiden. Die Creme muss gut einziehen/abtrocknen, es dürfen keine Rückstände zwischen den Zehen verbleiben.
- Nur Feilen verwenden, keine Raspeln, Nagelzwicker oder Scheren verwenden.
- Fußnägel spatenförmig (gerade) mit Feilen formen, nie schneiden – wegen Verletzungsgefahr.
- Keine Hühneraugenpflaster oder -tinkturen verwenden, sie können ätzende Stoffe enthalten, die zu Verletzungen führen.
- Bequeme, weite und weiche Schuhe tragen, möglichst aus Leder, keine Gummi- und Turnschuhe wegen der Schweißbildung. Schuhe täglich vor der Benutzung mit der Hand auf Unebenheiten oder Steinchen etc. kontrollieren.
- Baumwollstrümpfe ohne drückende Naht tragen, Strümpfe täglich wechseln
- Füße nicht großer Hitze aussetzen, wie sie etwa bei Heizdecken oder Kaminen entsteht, es besteht Verletzungsgefahr, keine direkte Sonneneinstrahlung
- Vorsicht beim Barfußlaufen, Fußpilzgefahr sowie Gefahr von Schnitt- und Schürfwunden
Besonders Diabetiker sollten bei Fußproblemen professionelle Hilfe bei einem Podologen, der sich auf die Behandlung von Diabetischem Fußsyndrom spezialisiert hat, suchen. Diese Behandlung kann unter bestimmten Voraussetzungen zu Lasten der gesetzlichen Krankenversicherung vom Arzt verordnet werden.
DFS Fußpass
Die Deutsche Diabetes Gesellschaft (DDG) entwickelte im Jahr 2020 gemeinsam mit der Deutschen Diabetes Hilfe, der Deutschen Gesellschaft für Angiologie und der Deutschen Gesellschaft für Gefäßchirurgie einen "DFS-Fußpass".[19] Dieser ist in drei Editionen erhältlich, die nach dem "Ampelsystem" (grün/gelb/rot) gestaffelt sind:
- grün für nicht sonderlich gefährdete Patienten: zur Vorsorge jährlich den Arzt aufsuchen
- gelb für gefährdete Patienten: mindestens halbjährliche Untersuchung
- rot für besonders gefährdete Patienten: alle drei Monate das DFS auf Veränderungen kontrollieren lassen
Der DFS-Fußpass kann von Ärzten über die beteiligten Fachgesellschaften geordert werden. Hinzu kommen entsprechend gefärbte Sticker, mit denen beispielsweise Patientenakten markiert werden können.
Behandlung
Je nach Schwere der Schädigung und des Stadiums sollten die Patienten fachgerecht von einem Wundbehandlungsteam versorgt werden. Durch die Wundheilungsstörung kann sich die Behandlung über sehr lange Zeiträume hinweg ziehen. Grundlegende Voraussetzung für die erfolgreiche Behandlung eines diabetischen Fußsyndroms ist die Druckentlastung der betroffenen Region, insbesondere der Wunde. Erst wenn die Entlastung des Fußes gewährleistet ist, können weitere therapeutische Maßnahmen greifen.[20] In einigen Fällen ist auch eine antibiotische Langzeittherapie zusätzlich zur regelmäßigen Wundversorgung notwendig. Ab Stadium II ist in Einzelfällen eine stationäre Versorgung notwendig. Die Behandlung kann sich an den Leitlinien der Deutschen Gesellschaft für Wundheilung und Wundbehandlung bzw. der Deutschen Diabetes-Gesellschaft orientieren. Im Wundbehandlungsteam arbeiten zur optimalen Versorgung je nach Fall unterschiedliche Spezialisten zusammen, u. a. Ärzte (Allgemeinarzt, Internist, Diabetologe, Chirurg, Gefäßchirurg, Orthopäde), auf Wundversorgung spezialisierte Pflegefachkräfte, Orthopädieschuhmacher und Podologen.
IRAS-Regel
Eine Orientierung zur Behandlung des diabetischen Fußsyndroms bietet das sogenannte IRA-Prinzip. Dieses Akronym setzt sich aus den Anfangsbuchstaben der Begriffe Infektbekämpfung, Revaskularisation und Amputation zusammen.[8] Ergänzt um den Aspekt der Schulung von Patienten und Angehörigen, erweitert sich dieses Prinzip zur IRAS-Regel.[21]
- Infektsanierung: Die Infektion ist beim DFS einer der entscheidenden Faktoren für die Gewebeschädigung. Eine Diagnose erfolgt klinisch und orientiert sich an IDSA oder PEDIS, den beiden gebräuchlichen Klassifikationen von Fußinfektionen im Zusammenhang mit Diabetes.
- Revaskularisation: Anhand des Knöchel-Arm-Index und der Messung der Verschlussdrücke der Fußarterien lässt sich auf den Status der Blutgefäße schließen. Deren Sanierung ist grundlegender Bestandteil der Therapie und die Voraussetzung für die Abheilung diabetischer Fußulcera.
Zeitnahe Infektbekämpfung und unverzügliche Revaskularisation sind die Voraussetzung für die Verhinderung weiterer Gewebeverluste. Setzen diese Maßnahmen erst verzögert ein, steigt das Risiko einer Amputation.[22]
- Amputation: Diabetiker unterliegen einem drei- bis zehnmal höheren Risiko einer Beinamputation als Nichtdiabetiker. Zwischen 50 und 70 % aller Amputationen an den unteren Extremitäten gehen auf eine diabetische Stoffwechselstörung zurück. 85 % der Fußamputationen bei Diabetikern sind auf ein DFS zurückzuführen, in dessen Folge sich eine Infektion entwickelte oder ein Gangrän ausbildete.[23]
- Schulung
Entlastung und Ruhigstellung
Ein weiterer wesentlicher Aspekt der Versorgung von Fußwunden bei Diabetikern ist die adäquate Druckentlastung des geschädigten Gewebes. Eine Wunde, auf die durch Kleidung, Bewegung und Eigengewicht des Patienten wiederholt oder beständig Druck ausgeübt wird, kann nicht störungsfrei abheilen und droht, zu einer chronischen Wunde zu werden. Die für die alltägliche Druckentlastung am besten untersuchte Methode ist das Entlasten des Fußes durch einen sogenannten Total Contact Cast. Hierbei handelt es sich um einen Vollkontakt-Gipsverband, der so anmodelliert wird, dass das geschädigte Gewebe beim Gehen nicht belastet wird. Der nicht abnehmbare Total Contact Cast gilt als Goldstandard der Versorgung von diabetischen Fußulzera.[24] Total Contact Casts, die aufgesägt werden und zum An- und Ablegen aus zwei Schalen bestehen, die mit einer einzelnen Gipsbinde oder mit Klettriemen befestigt werden, ermöglichen die Wundkontrolle und behindern den Betroffenen nicht bei der Körperpflege. Neben solchen TCC können Orthesen aus Kunststoff, Unterarm-Gehstützen oder ein Rollstuhl zum Einsatz kommen. In einigen Fällen kann anfänglich eine völlige Immobilisation des Betroffenen angeraten sein. Insbesondere bei älteren Patienten erhöht eine solche totale Ruhigstellung allerdings das Risiko der Entwicklung von Thrombosen und Pneumonien.
Selbst unter optimalen Bedingungen befinden sich viele Menschen mit Diabetischem Fußsyndrom in Dauerbehandlung und sind teilweise sehr eingeschränkt in den Aktivitäten des täglichen Lebens.
Therapiemethoden
Ursachenbekämpfung: Die Durchblutung kann durch gefäßchirurgische Maßnahmen, wie beispielsweise eine Revaskularisation durch einen Bypass verbessert werden. Orthopädische Eingriffe können Fehlstellungen im Bereich des Fußes korrigieren und lokale Überlastungen mit Druckbelastungsspitzen bei vorstehenden Knochen vermindern. Dazu bieten sich besonders bei der Osteoarthropathie korrigierende Gelenkversteifungen (Arthrodesen), korrigierende Knochenumstellungen (Korrekturosteotomien), partielle Knochenresektionen und Sehnenverlagerungen an.
Wundreinigung und Débridement: Meist chirurgische Abtragung von avitalem Gewebe, Nekrosen, Belägen oder Entfernung von Fremdkörpern bis an intakte anatomische Strukturen heran unter Erhalt von Granulationsgewebe – vorwiegend aktive periodische Wundreinigung als gezielte wiederkehrende mechanische Wundreinigung im Rahmen des Verbandwechsels.
Verbände: In einem Cochrane-Review zeigte sich im Jahr 2015 hinsichtlich der Wundheilung bei Patienten mit der Grunderkrankung Diabetes mellitus kein statistisch signifikanter Unterschied zwischen Hydrokolloiden und Gazen oder Kompressen, Alginaten, Schaumstoffen oder Hydrokolloiden unterschiedlicher Hersteller. Es wurde konstatiert, dass die Entscheidung für eine bestimmte Wundauflage sich an den Vorgaben der versorgenden Einrichtung, den wirtschaftlichen Erfordernissen und den individuellen Präferenzen des Patienten orientieren solle.[25] Als wirksame Versorgungsform gilt zudem die Vakuumtherapie, bei der die Wunde mit Unterdruck behandelt wird.[26]
Physikalische Interventionen: Zur Ergänzung der konventionellen Wundbehandlung werden eine ganze Reihe unterschiedlicher Verfahren angeboten, deren Ziel eine effektivere und schnellere Wundheilung ist, um hierdurch die überaus hohe Amputationsrate zu reduzieren. Neben vielen Fallberichten gibt es nur wenige gute klinische Studien, die wissenschaftlich eine tatsächliche Wirkung dieser Verfahren belegen. Viele Verfahren sind noch als experimentell zu bewerten. Eine Übersicht über die Wertigkeit der unterschiedlichen Behandlungsvorschläge findet sich laut einer Leitlinie der Deutschen Gesellschaft für Wundbehandlung (DGfW). Zu den dort genannten Verfahren gehören neben vielen anderen die Hyperbare Sauerstofftherapie[27][28], die Reizstromtherapie, die Ultraschalltherapie oder die Plasmatherapie[29][30][31].
Kontrolluntersuchungen Die Deutsche Diabetes-Gesellschaft empfiehlt mindestens einmal jährliche Kontrolluntersuchungen, wenn keine sensorische Neuropathie vorliegt, sonst alle sechs Monate. Bei Vorliegen einer arteriellen Verschlusskrankheit oder einer Fußdeformität sollte die Kontrolluntersuchung bereits alle drei Monate erfolgen, ebenso bei Frühstadien eines Ulkus. Doppler-Ultraschall-Kontrollen werden generell einmal jährlich empfohlen.[32]
Literatur
- Dirk Hochlenert, Gerald Engels, Stephan Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie. Springer Verlag, Berlin / Heidelberg 2014, ISBN 978-3-662-43943-2
- Franz X. Köck, Bernhard Koester (Hrsg.): Diabetisches Fußsyndrom. Georg Thieme Verlag, Stuttgart / New York 2007, ISBN 978-3-13-140821-1
- Kerstin Protz: Moderne Wundversorgung. 8. Auflage. Elsevier Urban & Fischer Verlag, München 2016, ISBN 978-3-437-27885-3
Weblinks
- Broschüre zur Fußgesundheit bei Diabetes mellitus. (PDF; 1,5 MB) Informationen für Patienten und Angehörige auf der Website des Wundzentrum Hamburg e. V.; abgerufen am 5. Dezember 2019
- Patienteninformationen zu Füßen bei Diabetes. Website des Ärztlichen Zentrums für Qualität in der Medizin (ÄZQ); abgerufen am 14. Oktober 2016
- Diabetisches Fußsyndrom, Kurzdefinition, Entstehung und Verlauf. Informationen des Deutschen Diabetes-Zentrums (DDZ) auf der diabetes-heute-Plattform der Universität Düsseldorf
- Leitlinie Diagnostik, Therapie, Verlaufskontrolle und Prävention des diabetischen Fußsyndroms. (PDF) S3-Leitlinie auf der Website der Deutschen Diabetesgesellschaft (DDG); abgerufen am 14. Oktober 2016
- Nationale VersorgungsLeitlinie Typ-2-Diabetes: Präventions- und Behandlungsstrategien für Fußkomplikationen. Stand: 30. November 2006 (in Überarbeitung); abgerufen am 6. Januar 2017
Einzelnachweise
- ↑ a b D. Hochlenert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie. Springer Verlag, Berlin / Heidelberg 2014, S. 7
- ↑ Holger Lawall: Diabetisches Fuß-Syndrom über Polyneuropathie, Durchblutungsstörungen und Zweitmeinungen. In: Deutscher Gesundheitsbericht Diabetes 2017 Die Bestandsaufnahme, Deutsche Diabetes Gesellschaft (DDG) und Diabetes DE – Deutsche Diabetes-Hilfe. Kirchheim, Mainz 2017
- ↑ Ernst-Adolf Chantelau: Quantitativer Nadelschmerz-Test (Pieks-Test) zeigt Prädisposition für diabetisches Fußsyndrom. (pdf) In: Zeitschrift für Allgemeinmedizin Band 98. 2022, S. 137–142, abgerufen am 2. Mai 2022.
- ↑ D. Hochlenert, G. Engels, G. Rümenapf, S. Morbach: Diabetisches Fußsyndrom. In: Der Diabetologe. Band 11, 2015, S. 151–163, doi:10.1007/s11428-014-1328-z
- ↑ a b K. Protz: Moderne Wundversorgung. 8. Auflage. Elsevier Urban & Fischer Verlag, München 2016, S. 146–149.
- ↑ a b c Matthias Augustin, Eike Sebastian Debus u. A.: Optimierte Wundtherapie und -pflege „UKE-Wundfibel“ Standards in der Diagnostik und Therapie von Wunden, Universitätsklinikum Hamburg-Eppendorf, 3. Auflage 2015, Seite 22
- ↑ a b Alphabetisches Verzeichnis zur ICD-10-WHO Version 2019, Band 3. Deutsches Institut für Medizinische Dokumentation und Information (DIMDI), Köln, 2019, S. 149.
- ↑ a b Hans Lippert: Wundatlas. Kompendium der komplexen Wundbehandlung. Georg Thieme Verlag, Stuttgart 2006, ISBN 3-13-140832-4, S. 222–233
- ↑ Nationale VersorgungsLeitlinie Typ-2-Diabetes: Präventions- und Behandlungsstrategien für Fußkomplikationen Stand: 30. November 2006 (in Überarbeitung)
- ↑ a b D. Hochlenert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie.Springer Verlag, Berlin / Heidelberg 2014, S. 5–7
- ↑ K. Hodeck, A. Bahrmann (Hrsg.): Pflegewissen Diabetes. Springer Verlag 2014, S. 77
- ↑ Neuropathisch-infizierter Fuß (62 %).
- ↑ Makroangiopathisch-ischämischer Fuß (13 %).
- ↑ Neuropathisch-ischämischer Fuß (25 %).
- ↑ Richard Daikeler, Götz Use, Sylke Waibel: Diabetes. Evidenzbasierte Diagnosik und Therapie. 10. Auflage. Kitteltaschenbuch, Sinsheim 2015, ISBN 978-3-00-050903-2, S. 150.
- ↑ N. C. Schaper: Diabetic foot ulcer classification system for research purposes: a progress report on criteria for including patients in research studies. In: Diabetes Metab Res Rev, 2004, 20(Suppl 1), S. S90–S95. International Working Group on the Diabetic Foot (IWGDP) (PDF)
- ↑ D. Hochlenert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie. Springer Verlag, Berlin / Heidelberg 2014, ISBN 978-3-662-43943-2, S. 2
- ↑ K. Hodeck, A. Bahrmann: Pflegewissen Diabetes. Springer Verlag, Berlin / Heidelberg 2014, ISBN 978-3-642-38408-0, S. 79
- ↑ Neuer Fußpass kostenfrei von der DDG auf diabetesnews.de, aufgerufen am 1. Februar 2021
- ↑ K. Protz: Moderne Wundversorgung. 8. Auflage. Elsevier Urban & Fischer Verlag, München 2016, S. 162
- ↑ Kerstin Protz: Moderne Wundversorgung. 8. Auflage. Elsevier Urban & Fischer Verlag, München 2016, S. 260
- ↑ D. Hochlenert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie. Springer Verlag, Berlin / Heidelberg 2014, ISBN 978-3-662-43943-2, S. 60
- ↑ Holger Lawall: Diabetisches Fuß-Syndrom über Polyneuropathie, Durchblutungsstörungen und Zweitmeinungen, in Deutscher Gesundheitsbericht Diabetes 2017 Die Bestandsaufnahme, Deutsche Diabetes Gesellschaft (DDG) und Diabetes DE – Deutsche Diabetes-Hilfe, Kirchheim, Mainz 2017
- ↑ D. Hochlehnert, G. Engels, S. Morbach: Das diabetische Fußsyndrom – Über die Entität zur Therapie, Springer Verlag, Heidelberg 2014, ISBN 978-3-662-43943-2, S. 128
- ↑ L. Wu, G. Norman, J.C. Dumville, S. O’Meara, S.E. Bell-Syer: Dressings for treating foot ulcers in people with diabetes: an overview of systematic reviews. The Cochrane Database of systematic Reviews, 2015, Art. No.: CD010471
- ↑ D. Seidel, E.A.M. Neugebauer, R. Liefering, T. Mathes, W. Eglmeier, A. Hörster, S. Banaoglu, V. Jakob, A. Staß, S, Ashoori, U. Schwanke, P. Krüger, F. Schwarzkopf: Ausweg aus der Evidenzfalle. Randomisierte, kontrollierte Studie zur Unterdruck-Wundtherapie bei Diabetischen Fußwunden im Auftrag der gesetzlichen Krankenkassen. In: Zeitschrift für Wundheilung, 1/2013, S. 15–21, ISSN 1439-670X
- ↑ Nach Urteil des Bundessozialgerichtes vom 7. Mai 2013 (PDF; 23 kB) können in Deutschland dafür geeignete gesetzlich versicherte Patienten bei entsprechender Diagnosestellung den Kostenersatz von ihrer Krankenkasse erhalten
- ↑ Deutsche Diabetes Gesellschaft kritisiert IQWiG-Einschätzung zur HBO beim diabetischen Fußsyndrom: Schnellerer Wundverschluss durch Hyperbare Sauerstofftherapie (HBO) ist nicht ausreichend belegt. Deutsche Diabetesgesellschaft, abgerufen am 16. November 2016.
- ↑ Stephanie Arndt, Anke Schmidt, Sigrid Karrer, Thomas von Woedtke: Comparing two different plasma devices kINPen and Adtec SteriPlas regarding their molecular and cellular effects on wound healing. In: Clinical Plasma Medicine. Band 9, März 2018, S. 24–33, doi:10.1016/j.cpme.2018.01.002 (elsevier.com [abgerufen am 15. April 2020]).
- ↑ F. Brehmer, H.A. Haenssle, G. Daeschlein, R. Ahmed, S. Pfeiffer: Alleviation of chronic venous leg ulcers with a hand-held dielectric barrier discharge plasma generator (PlasmaDerm ® VU-2010): results of a monocentric, two-armed, open, prospective, randomized and controlled trial (NCT01415622). In: Journal of the European Academy of Dermatology and Venereology. Band 29, Nr. 1, Januar 2015, S. 148–155, doi:10.1111/jdv.12490 (wiley.com [abgerufen am 15. April 2020]).
- ↑ Thoralf Bernhardt, Marie Luise Semmler, Mirijam Schäfer, Sander Bekeschus, Steffen Emmert: Plasma Medicine: Applications of Cold Atmospheric Pressure Plasma in Dermatology. 2019, abgerufen am 15. April 2020 (englisch).
- ↑ Holger Lawall: Diabetisches Fuß-Syndrom über Polyneuropathie, Durchblutungsstörungen und Zweitmeinungen, in Deutscher Gesundheitsbericht Diabetes 2017 Die Bestandsaufnahme, Deutsche Diabetes Gesellschaft (DDG) und Diabetes DE – Deutsche Diabetes-Hilfe, Kirchheim, Mainz 2017