Amitriptylin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
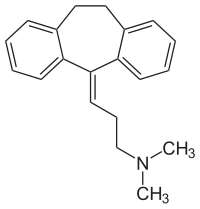
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Amitriptylin | ||||||||||||||||||
| Andere Namen |
3-(10,11-Dihydro-5H-dibenzo[a,d]cyclohepten-5-yliden)-N,N-dimethylpropylamin | ||||||||||||||||||
| Summenformel |
| ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| ATC-Code | |||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Wirkmechanismus |
| ||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse |
| ||||||||||||||||||
| Schmelzpunkt |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Amitriptylin ist ein Arzneistoff aus der Gruppe der trizyklischen Antidepressiva, der in erster Linie zur Behandlung von Depressionen und zur langfristigen Schmerzbehandlung eingesetzt wird. In einer Übersichtsstudie von 2001 wurde es als „Goldstandard-Antidepressivum“ bezeichnet.[3]
Geschichte
Amitriptylin wurde 1960 erstmals synthetisiert und 1962 vom Arzneimittelhersteller Lundbeck am Markt eingeführt. Es war lange Jahre – bis zum Aufkommen der Serotonin-Wiederaufnahmehemmer – das meistverordnete Antidepressivum weltweit. 2011 stand Amitriptylin immer noch an 4. Stelle der meistverordneten Psychopharmaka in Deutschland.[4]
Klinische Angaben
Anwendungsgebiete (Indikationen)
Amitriptylin-Präparate sind zur Behandlung von Depressionen zugelassen. Sie werden gegen alle Formen depressiver Erkrankungen eingesetzt, bevorzugt gegen solche, die überwiegend mit Angst und Unruhegefühlen einhergehen. Ein weiteres zugelassenes Anwendungsgebiet des die Schmerzwahrnehmung vermindernden Medikaments ist die langfristige Schmerzbehandlung im Rahmen eines therapeutischen Gesamtkonzeptes.[5]
Auf Grund seiner migräneprophylaktischen Wirkung gilt Amitriptylin als Mittel der ersten oder zweiten Wahl bei der Prophylaxe der Migräne.[6][7] Auch zur vorbeugenden Behandlung des Spannungskopfschmerzes gilt Amitriptylin als der am besten untersuchte Arzneistoff.[8] Demgegenüber liegen für eine mögliche Anwendung zur Langzeitbehandlung der Trigeminusneuralgie kaum Daten vor.[9]
Außerhalb der zugelassenen Anwendungsgebiete wird das auch sedierend wirkende Amitriptylin häufig auch als Hypnotikum bei Schlafstörungen eingesetzt. Seine Wirksamkeit gilt jedoch als wenig belegt.[10] Wie andere trizyklische Antidepressiva ist es auch zur Behandlung des Reizdarmsyndroms[11] und der Fibromyalgie[12] wirksam. Darüber hinaus scheint Amitriptylin zur Behandlung der posttraumatischen Belastungsstörung (PTBS) geeignet zu sein.[13] Diese Anwendungsgebiete außerhalb der arzneimittelrechtlichen Zulassung stellen jedoch einen sogenannten Off-Label-Use dar.
Gegenanzeigen (Kontraindikationen)
Neben einer bekannten Überempfindlichkeit gegen den Wirkstoff gelten die Anwendung in der unmittelbaren Genesungsphase nach einem Herzinfarkt, Erregungsleitungsstörungen im His-Bündel, akuter Harnverhalt, Pylorusstenose, Darmverschluss, unbehandeltes Engwinkelglaukom sowie akute Alkohol-, Barbiturat- und Opiatvergiftung als absolute Kontraindikationen.[5]
Auf Grund der Gefahr eines möglicherweise lebensbedrohlichen Serotonin-Syndroms darf Amitriptylin nicht gleichzeitig mit MAO-Hemmern angewendet werden. Bei einem Therapiewechsel ist ein zeitlicher Sicherheitsabstand zu beachten. Wegen der Gefahr unerwünschter Herzwirkungen, wie Arrhythmien und Erregungsleitungsstörungen, ist die gleichzeitige Anwendung von Amitriptylin mit Arzneimitteln, die, wie beispielsweise Cisaprid, die QT-Zeit verlängern, kontraindiziert.[5]
Sonstige Schäden des Herz-Kreislaufsystems, Hyperthyreose, eingeschränkte Leberfunktion, Epilepsie, unbehandeltes Engwinkelglaukom, Harnverhalt, Prostatahyperplasie und paranoide oder prädelirante Zustandsbilder gelten, wie auch der Einsatz bei Patienten unter 18 Jahren, als relative Anwendungsbeschränkungen.[5]
Anwendung in der Schwangerschaft und Stillzeit
Zur Anwendung von Amitriptylin in der Schwangerschaft liegen keine ausreichenden Erfahrungen vor. Tierversuche lassen vermuten, dass es möglicherweise zu Schädigungen des Fötus kommen kann. Amitriptylin sollte in der Schwangerschaft nur verwendet werden, wenn es unbedingt erforderlich ist.[5]
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Amitriptylin wirkt sedierend und kann damit einen ausgeprägten Einfluss auf die Fahrtüchtigkeit haben und auf die Fähigkeit, Maschinen zu bedienen.[5] Dies gilt in besonderem Maße bei Behandlungsbeginn, bei Präparatewechsel sowie im Zusammenwirken mit anderen zentral wirkenden Arzneimitteln (Schmerzmittel, Schlafmittel, Psychopharmaka) sowie bei gleichzeitiger Einnahme von Alkohol. Daher sollten das Führen von Fahrzeugen, die Bedienung von Maschinen oder sonstige gefahrvolle Tätigkeiten insbesondere während der ersten Tage der Behandlung unterlassen werden. Die Entscheidung ist im Einzelfall durch den behandelnden Arzt unter Berücksichtigung der individuellen Dosierung und der jeweiligen Reaktion zu treffen.
Wechselwirkungen
Die Kombination von MAO-Hemmern (z. B. Tranylcypromin) mit Amitriptylin kann zu dem lebensbedrohlichen Serotoninsyndrom führen. Auf Grund seines insbesondere bei hoher Dosis zu beobachtenden Potenzials, Herz-Rhythmusstörungen mit QT-Zeit-Verlängerung, Torsade de pointes und Sinustachykardien zu verursachen, besteht bei einem gleichzeitigen Einsatz von Amitriptylin und Arzneimitteln mit einer Wirkung auf die QT-Zeit eine erhöhte Gefahr von Herzrhythmus-Störungen. Diese Gefahr besteht auch bei gleichzeitiger Anwendung von Arzneimitteln, die zu einer Hypokaliämie führen, oder Arzneimitteln, welche die Verstoffwechslung von Amitriptylin über den Cytochrom-P450-Enzymkomplex CYP3A4 in der Leber hemmen. Dem gegenüber können Arzneistoffe, die, wie beispielsweise Carbamazepin und Phenytoin, dieses Enzymsystem induzieren, den Amitriptylinabbau beschleunigen und zu einer unzureichenden Amitriptylinwirkung führen.[5]
Auf Grund seiner inhibitorischen Wirkung auf Acetylcholin- und Histaminrezeptoren können die Wirkungen und Nebenwirkungen von Anticholinergika und Antihistaminika bei gleichzeitiger Einnahme mit Amitriptylin verstärkt werden. Ebenso verstärkt Amitriptylin die Effekte direkter Sympathomimetika. Die Wirkung von Antihypertensiva, wie Guanethidin, wird hingegen abgeschwächt.[5]
Nebenwirkungen
Zu den häufigsten Nebenwirkungen (> 10 %) unter der Anwendung von Amitriptylin gehören zentralnervöse Störungen wie Kopfschmerzen, Vertigo, Tremor und Schläfrigkeit, Störungen des Herz-Kreislauf-Systems wie Palpitation, Tachykardie und orthostatische Hypotonie, gastrointestinale Störungen wie Mundtrockenheit, Verstopfung und Übelkeit sowie Gewichtszunahme, Akkommodationsstörungen und Schwitzen.[5] Wie bei anderen trizyklischen Antidepressiva stehen insbesondere die unerwünschten anticholinergen Arzneimittelwirkungen im Vordergrund.
Zu den weiteren zentralnervös bedingten Nebenwirkungen zählen Parästhesie, Ataxie, Müdigkeit (1–10 %) und gelegentlich (0,1–1 %) Konvulsionen. Die häufigsten psychischen Störungen (1–10 %) sind Verwirrtheit, Konzentrationsschwierigkeiten und Libidoverminderung, gefolgt (0,1–1 %) von Hypomanie, Manie, Ängstlichkeit, paradoxer Schlaflosigkeit und Albträumen sowie seltener (< 0,1 %) Appetitlosigkeit, Delirien bei älteren Patienten und Halluzinationen bei schizophrenen Patienten. Am Herzen können häufig (1–10 %) EKG-Veränderungen wie QTc-Zeit-Verlängerung, AV-Block und Erregungsweiterleitungsstörungen beobachtet werden, die sich jedoch nur selten (< 0,1 %) als Arrhythmien äußern. Gelegentlich kann eine Hypotonie beobachtet werden. Eine bereits bestehende Herzinsuffizienz kann durch Amitriptylin verstärkt werden.[5] Über Risiken von peripheren Kältempfindungen an Händen und/oder Füßen bzw. das Auftreten des Raynaud-Syndroms berichtet die neuseeländische Arzneimittelsicherheitsbehörde Medsafe.[14]
Des Weiteren können unter anderem Geschmacksveränderung, Durchfall, Übelkeit und Erbrechen, Harnverhalten und Impotenz auftreten.[5]
Pharmakologie
Pharmakodynamik
Amitriptylin wirkt im Zentralnervensystem als relativ unselektiver Hemmstoff der Monoamin-Rückaufnahme aus dem synaptischen Spalt in die Präsynapse. Auf diese Weise erhöht sich die Konzentration von Neurotransmittern (vor allem Serotonin und Noradrenalin) im synaptischen Spalt. Man nimmt heute an, dass die Reduktion depressiver Symptome durch eine modifizierte Empfindlichkeit der Rezeptoren für Monoamine erklärt werden kann. Die Empfindlichkeitssteigerung beruht dabei auf einer Down-Regulation bestimmter monoaminerger Rezeptoren aufgrund der veränderten Konzentrationsverhältnisse. Dies ist zudem die Begründung dafür, dass der stimmungsaufhellende Effekt in der Regel erst nach einer gewissen Einnahmedauer (etwa zwei bis drei Wochen) eintritt.
Daneben hat Amitriptylin Effekte auf weitere Übertragungsprozesse im Gehirn, beispielsweise wirkt es anticholinerg (etwa als Antagonist bestimmter Acetylcholin-Wirkungen) und leicht antihistaminisch. Daraus resultiert eine psychomotorisch eher dämpfende Gesamtwirkung; außerdem treten charakteristische Nebenwirkungen auf. Die sedierende Wirkkomponente vermindert sich meistens im Laufe der Anwendungsdauer. Amitriptylin wirkt zudem als FIASMA (funktioneller Hemmer der sauren Sphingomyelinase).[15]
Die pharmakologische Wirksamkeit von Amitriptylin, trizyklischen Antidepressiva und allen natriumkanalblockierenden Antiepileptika bei neuropathischen Schmerzen (Gürtelrose) beruht auf der reversiblen kompetitiven Blockade von spannungsabhängigen Natriumkanälen, die hier durch autonome Spontanaktivität eine Schmerzgenese verursachen, wobei hier das pharmakologische Prinzip der „use-dependence“ die Nichtbeeinflussung physiologischer Aktionspotentiale erklärt, da nur die sich sehr schnell öffnenden pathophysiologischen und schmerzerzeugenden Natriumkanäle geblockt werden.
Der molekulare Wirkungsmechanismus kann durch das Prinzip der Ionenfalle (Lokalanästhetika) erklärt werden, wonach extrazelluläres Amitriptylin (pH = 7,4 (physiologisch)) im Gleichgewicht zwischen unprotonierter Form und protonierten Form vorkommt, aber nur die unprotonierte Form (freies Amin) die ausreichende Lipophilie besitzt, die notwendig ist, um die Doppellayer-Lipidmembran der Zelle nach intrazellulär zu penetrieren und sich hieran anschließend durch Protonierung in der Zelle zu akkumulieren. Die protonierte, positiv geladene und intrazellulär vorliegende Form von Amitriptylin gelangt durch Diffusion, umgeben durch eine Hydrathülle, zu den spannungsabhängigen Natriumkanälen (dendritisch, somatisch u. axonal), die durch Amitriptylin reversibel blockiert werden.
Die natriumkanalblockierenden bzw. lokalanästhetischen Eigenschaften von Amitriptylin können auch experimentell überprüft werden, indem man eine Tablette, die Amitriptylin beinhaltet, zerbricht und sich auf die Zunge legt, wobei sich eine lokale Betäubung wahrnehmen lässt.
Pharmakokinetik
Die Halbwertszeit im Körper beträgt 8–51 Stunden; die Halbwertzeit der Amitriptylin-Metaboliten 30 Stunden. Der Metabolit Nortriptylin ist ebenfalls wirkaktiv und wird selbst als Arzneimittel vertrieben.
Resorption
Nach oraler Gabe wird Amitriptylin langsam aber vollständig resorbiert. Auf Grund der häufig verzögerten Magen-Darm-Passage werden maximale Plasmakonzentrationen erst nach 1 bis 5 (max. 8) Stunden erreicht. Die systemische Bioverfügbarkeit beträgt im Verhältnis zur intravenösen Injektion etwa 50 %.[16]
Verteilung
Auf Grund seiner großen Lipophilie wird Amitriptylin im ganzen Organismus verteilt. Das Verteilungsvolumen beträgt 14 bis 18 l/kg. Amitriptylin wird stark an Gewebs- und Plasmaeiweiße gebunden; nur 3 – 6 % liegen frei im Plasma vor (der aktive Metabolit Nortriptylin zu 8 – 13 %). Sowohl Amitriptylin als auch Nortriptylin treten in die Muttermilch über.[16]
Biotransformation
Amitriptylin wird hauptsächlich in der Leber metabolisiert. Bei therapeutischen Konzentrationen erfolgt der Metabolismus von Amitriptylin vorwiegend durch Demethylierung (CYP2C19) und Hydroxylierung (CYP2D6), gefolgt von Konjugation mit der Glukuronsäure. Der durch N-Demethylierung entstehende Hauptmetabolit Nortriptylin ist ebenfalls pharmakologisch aktiv. Amitriptylin und Nortriptylin werden anschließend hydroxyliert; die entstehenden 10-Hydroxy-Metaboliten besitzen noch etwa die Hälfte der biologischen Aktivität von Amitriptylin. Etwa 5 – 14 % der kaukasischen Bevölkerung sind auf Grund genetisch bedingter Unterschiede im Cytochrom P450-System CYP2D6 „poor metabolizer“. Bei diesen Patienten können deshalb sehr hohe Plasmaspiegel auftreten. Offenbar auf Grund verminderter Biotransformation treten bei älteren Patienten höhere Plasmakonzentrationen auf.[16]
Elimination
Die Ausscheidung der Metaboliten erfolgt in freier oder konjugierter Form. Unverändertes Amitriptylin wurde nur in geringen Mengen im Urin gefunden. Die Plasma-Halbwertszeit von Amitriptylin beträgt nach oraler Gabe ca. 10 bis 28 Stunden; bei älteren Menschen ist die Halbwertszeit verlängert. Die Plasma-Clearance wird mit 0,17–0,32 l/kg/h und für ältere Probanden mit 0,18–0,45 l/kg/h angegeben.[16]
Pathophysiologische Variationen
Bei Patienten mit Niereninsuffizienz ist die Konzentration an unkonjugierten Metaboliten im Plasma gegenüber nierengesunden Patienten verringert, dagegen ist die Konzentration an konjugierten Metaboliten stark erhöht.[16]
Toxikologie
In vitro blockiert Amitriptylin exprimierte hERG-Kanäle in mikromolaren Konzentrationen, die im oberen Bereich therapeutischer Plasmakonzentrationen liegen. Diese Kanäle sind für die Repolarisation im Herzen verantwortlich. Daher hat Amitriptylin das Potenzial, bestimmte Formen von Kammerherzrhythmusstörungen (Torsades de pointes) auszulösen.
Das genotoxische Potential von Amitriptylinhydrochlorid wurde in verschiedenen in vitro und in vivo Testsystemen untersucht. Obwohl die Ergebnisse zum Teil widersprüchlich sind, kann ein genotoxisches Potential, insbesondere im Hinblick auf mögliche Schädigungen von Chromosomen, nicht ausgeschlossen werden. Langzeituntersuchungen auf ein tumorerzeugendes Potenzial wurden nicht durchgeführt.
In Untersuchungen zur Reproduktionstoxizität wurden nach sehr hohen Dosen bei verschiedenen Tierspezies fetotoxische und teratogene Effekte beobachtet. Von anderen Antidepressiva liegen Hinweise auf Verhaltensstörungen der pränatal exponierten Nachkommen im Tierexperiment vor. Für Amitriptylin sind keine entsprechenden Angaben bekannt.[16]
Handelsnamen
- Monopräparate
- Saroten (D, A, CH), Amineurin (D), Syneudon (D), Tryptizol (D), zahlreiche Generika (D)
- weitere Handelsnamen: Elavil (weltweit), Laroxyl (weltweit), Endep (AUS, CDN, NZ, ZA)
- Kombinationspräparate
- Limbatril (D), Limbitrol (CH): Amitriptylin + Chlordiazepoxid (In den 1970er und 1980er Jahren eines der beliebtesten Psychopharmaka)
Es wird als Tablette, Dragée oder Lösung oral eingenommen, kann aber auch als Injektionslösung i. m. oder i. v. appliziert werden.
Einzelnachweise
- ↑ a b c Datenblatt Amitriptylinhydrochlorid bei Sigma-Aldrich, abgerufen am 29. Mai 2022 (PDF).
- ↑ a b c d e f g A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances – Synthesis, Patents, Applications. 4. Auflage. Thieme-Verlag, Stuttgart 2000, ISBN 1-58890-031-2.
- ↑ C. Barbui, M. Hotopf: Amitriptyline v. the rest: still the leading antidepressant after 40 years of randomised controlled trials. In: The British Journal of Psychiatry: The Journal of Mental Science. Band 178, Februar 2001, S. 129–144, PMID 11157426.
- ↑ U. Schwabe, D. Paffrath (Hrsg.): Arzneiverordnungs-Report 2012. Berlin-Heidelberg: Springer-Verlag, 2012. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ a b c d e f g h i j k Fachinformation des Arzneimittel-Kompendiums der Schweiz: Saroten retard; Stand: September 2006.
- ↑ S. D. Silberstein: Practice parameter: evidence-based guidelines for migraine headache (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. In: Neurology. Band 55, Nr. 6, September 2000, S. 754–762, PMID 10993991.
- ↑ S. Evers, A. May, G. Fritsche, P. Kropp, C. Lampl, V. Limmroth, V. Malzacher, S. Sandor, A. Straube, H. C. Diener: Akuttherapie und Prophylaxe der Migräne – Leitlinie der Deutschen Migräne- und Kopfschmerzgesellschaft und der Deutschen Gesellschaft für Neurologie. In: Nervenheilkunde. Band 27, Nr. 10, 2008, S. 933–949 (dmkg.de [PDF]).
- ↑ M. E. Bigal, A. M. Rapoport, R. Hargreaves: Advances in the pharmacologic treatment of tension-type headache. In: Curr Pain Headache Rep. Band 12, Nr. 6, Dezember 2008, S. 442–446, PMID 18973738.
- ↑ L. He, B. Wu, M. Zhou: Non-antiepileptic drugs for trigeminal neuralgia. In: Cochrane Database Syst Rev. Band 3, 2006, S. CD004029, doi:10.1002/14651858.CD004029.pub2, PMID 16856027.
- ↑ P. M. Becker: Pharmacologic and nonpharmacologic treatments of insomnia. In: Neurol Clin. Band 23, Nr. 4, November 2005, S. 1149–1163, doi:10.1016/j.ncl.2005.05.002, PMID 16243620.
- ↑ A. C. Ford, N. J. Talley, P. S. Schoenfeld, E. M. Quigley, P. Moayyedi: Efficacy of antidepressants and psychological therapies in irritable bowel syndrome: systematic review and meta-analysis. In: Gut. Band 58, Nr. 3, März 2009, S. 367–378, doi:10.1136/gut.2008.163162, PMID 19001059.
- ↑ N. Uçeyler, W. Häuser, C. Sommer: A systematic review on the effectiveness of treatment with antidepressants in fibromyalgia syndrome. In: Arthritis Rheum. Band 59, Nr. 9, September 2008, S. 1279–1298, doi:10.1002/art.24000, PMID 18759260.
- ↑ National Institute for Clinical Excellence: Post traumatic stress disorder: the management of PTSD in primary and secondary care. 2005. PMID 21834189
- ↑ Early Warning System – Monitoring Communication Archive. In: medsafe.govt.nz. Medsafe, abgerufen am 23. Juni 2016.
- ↑ J. Kornhuber, M. Muehlbacher, S. Trapp, S. Pechmann, A. Friedl, M. Reichel, C. Mühle, L. Terfloth, T. Groemer, G. Spitzer, K. Liedl, E. Gulbins, P. Tripal: Identification of Novel Functional Inhibitors of Acid Sphingomyelinase. In: PLoS ONE. Band 6, Nr. 8, 2011, S. e23852, doi:10.1371/journal.pone.0023852.
- ↑ a b c d e f fachinfo.deSaroten, abgerufen am 18. Juni 2019.