Polyester
| Allgemeine Struktur von Polyestern |
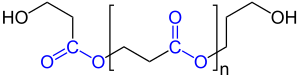
| Links: Wiederholeinheit bei Polyestern, die aus Lactonen hergestellt werden. Diese Polyester sind Carbonsäureester. Rechts: Wiederholeinheit bei Polycarbonaten, dies sind Kohlensäureester (Carbonate). Sie sind oft Kondensate aus Dihydroxyverbindungen und Phosgen [Cl–(CO)–Cl]. Die beiden unterschiedlichen Esterfunktionen sind blau gekennzeichnet. R steht für den „Rest“ der zur Synthese eingesetzten Verbindungen. |
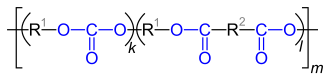
| Wiederholeinheiten von Polyestern, die aus Dicarbonsäuren und Dihydroxyverbindungen hergestellt werden. R1 steht für den „Rest“ der eingesetzten Dicarbonsäure, R2 für den „Rest“ der eingesetzten Dihydroxyverbindung. |
| Wiederholeinheiten bei Copolymeren von Carbonaten und Carbonsäureestern (Polyestercarbonate). R2 steht für den „Rest“ der eingesetzten Dicarbonsäure, R1 für den „Rest“ der eingesetzten Dihydroxyverbindung. |
Polyester sind Polymere mit Esterfunktionen in ihrer Hauptkette. Zwar kommen auch in der Natur Polyester vor, doch heute versteht man unter Polyester eher eine große Familie synthetischer Polymere (Kunststoffe), zu denen die viel verwendeten Polycarbonate (PC) und vor allem das technisch wichtige, thermoplastische Polyethylenterephthalat (PET)[1] gehören. Eine weitere Form sind ungesättigte Polyesterharze (UP-Harze), die durch Härtung zu Duroplasten werden und als preisgünstiges Matrixharz im Bereich Faserverbundkunststoffe verwendet werden. Außerdem lassen sich aromatische Polyester zu flüssigkristallinen Polymerketten anordnen, wodurch sich das Eigenschaftsprofil eines Hochleistungskunststoffes ergibt.
Geschichte
Natürliche Polyester sind seit etwa 1830 bekannt. Der erste synthetische Polyester Glycerinphthalat wurde im Ersten Weltkrieg als Imprägnierungsmittel verwendet; Alkydharze kamen als Glyptal bei General Electric in den 1920er Jahren auf den Markt.[2] Als Textilfaser wurden sie in der Gruppe von Wallace Hume Carothers bei DuPont entwickelt, allerdings waren diese noch nicht hitzebeständig, was erst John Rex Whinfield Anfang der 1940er Jahre in England gelang. Die erste solche Faser wurde bald nach dem Zweiten Weltkrieg als Terylene bei Imperial Chemical Industries produziert.[3]
Anwendungen

- Polyesterfaserstoffe (PES) für Textilien, Vliesstoffe und Mikrofasern
- PET-Flaschen
- Folien, z. B. kopierfähige Folie für Tageslichtprojektoren, Basismaterial für flexible Leiterplatten (biaxial orientierte Polyester-Folien), Dielektrikum für Kondensatoren
- fotografische Filme (neben Cellulose-Triacetat ist Polyester das wichtigste Trägermaterial)
- ungesättigte Polyesterharze für Gießharze und Faserverbundwerkstoffe
- als Alkydharze für Lacke
- Polyesterpolyole dienen als Rohstoff bei der Reaktion von Diisocyanaten zu Polyurethanen.
Kurzbezeichnungen
- PBT: Polybutylenterephthalat, ein Polymer der Terephthalsäure
- PET: Polyethylenterephthalat, ein Polymer der Terephthalsäure
- PLA: Polylactid, das biologisch abbaubare Polymer der Milchsäure. Das Polymer der D-(−)-Milchsäure wird auch mit PDLA abgekürzt, das der L-(+)-Milchsäure mit PLLA. PDLLA ist die Poly-D,L-Milchsäure.[4]
- PTT: Polytrimethylenterephthalat
- PEN: Polyethylennaphthalat
- PC: Polycarbonat, ein Ester der Kohlensäure
- PEC: Polyestercarbonat, sowie Carbonsäureester, als auch Ester der Kohlensäure
- PAR: Polyarylate, aromatische Polyester
- UP: ungesättigtes Polyesterharz
Synthese
Allgemein erfolgt die Polyestersynthese in einer Polykondensationsreaktion oder durch ringöffnende Polymerisation.
Azeotrope Veresterung
Die Azeotrope Veresterung ist eine klassische (Labor-)Methode, bei der ein Alkohol und eine Carbonsäure zu einem Carbonsäureester reagieren. Um ein Polymer aus Diol und Dicarbonsäure herzustellen, muss das bei der Reaktion entstehende Wasser ständig durch azeotrope Destillation entfernt werden, um das chemische Gleichgewicht auf die Esterseite zu verschieben. Die Reaktion wird von Titan- oder Zinn(IV)-alkoholaten bei 180–240 °C katalysiert. Man kann ca. 2 % Xylol als Wasserschlepper zusetzen. Durch geeignete Wahl der Edukte kann man Hydroxygruppen-haltige Polyester erzeugen. Der Veresterungsgrad ist üblicherweise > 95 %, bestimmt durch eine begleitende Säurezahl-Bestimmung.
Umesterung
Bei der Umesterung wird ein Diol in der Schmelze am Katalysatorkontakt mit einem Dicarbonsäureester (z. B. Dimethylterephthalat) umgesetzt. Mit dieser Methode werden die Massenkunststoffe Polybutylenterephthalat (PBT) und Polyethylenterephthalat (PET) hergestellt.
Carbonsäurechloridmethode
Anstatt Carbonsäuren werden Carbonsäurechloride verwendet. Die Polykondensation geschieht so unter Abspaltung von Chlorwasserstoff (HCl) anstelle von Wasser. Diese Acylierungsmethode kann in Lösungsmitteln, als Interphasen- oder als Schmelzreaktion erfolgen.
- Silylmethode
- In dieser Variante der Salzsäuremethode wird das Carbonsäurechlorid mit dem Trimethylsilylether der Alkoholkomponente umgesetzt; es wird Trimethylsilylchlorid abgespalten.
Acetatmethode (Umesterung)
In dieser nur für phenolische Hydroxygruppen geeigneten Methode reagiert die Säure mit der bereits mit Essigsäure veresterten Alkoholkomponente. Bei der Kondensation entsteht Essigsäure, die nicht so einfach wie Wasser oder Salzsäure zu entfernen ist, wodurch der pH-Wert sinkt und es häufig zu sauren Nebenreaktionen kommt.
- Silylacetatmethode
- In dieser Variante der Acetatmethode wird nicht die Carbonsäure, sondern deren Trimethylsilylester verwendet. Es entsteht der Essigsäuretrimethylsilylester, der nicht sauer ist.
Ringöffnende Polymerisation
Bei der ringöffnenden Polymerisation können aus Lactonen über anionische, kationische, koordinative Kettenpolymerisation oder Enzym-basiert[5] ohne Kondensationsreaktion unter sehr milden Bedingungen aliphatische Polyester hergestellt werden.
Handelsnamen
Fasern, Gewebe sowie Fleecestoffe (Faserpelz) aus Polyester werden unter verschiedenen Handelsnamen vertrieben:[6]
- Polarguard
- Thermolite
- Trevira
- Dacron
- Diolen
- Sorona, ein PTT von DuPont, welches auf biobasiertem 1,3-Propoandiol (PDO) basiert.
- Terylene
- Vestan
- Grisuten[7]
- Tritan
Polyester- bzw. PET-Folien sind hervorragende Dielektrika und Isolierstoffe. Daraus hergestellte Folienkondensatoren haben das Kürzel MKS (WIMA) bzw. MKT (epcos/TDK). Siehe auch Biaxial orientierte Polyester-Folie (Mylar).
Polyesterlack
Polyesterlacke sind Lösungen ungesättigter Polyester (z. B. Maleinsäureglycolester) in einem Monomer (z. B. Styrol), dem man organische Peroxide als Reaktionsbeschleuniger zusetzt. Polyesterlacke werden als lösungsmittelfreie oder lösungsmittelarme Lacke verwendet. Die erhaltenen Filme besitzen eine hohe Witterungs- und Chemikalienbeständigkeit. Das Hauptverwendungsgebiet der Polyesterlacke bildet die Herstellung von farblosen und pigmentierten Holzlacken sowie von Spachtelmassen für Holz und Eisen. Darüber hinaus wird Polyester in der Herstellung und Anwendung von Pulverlacken gebraucht.[8]
Ökologische Auswirkungen
Polyester erzeugt in mehrfacher Hinsicht Umweltprobleme:
- Die Herstellung beruht auf Erdöl; die Herstellung ist energie- und wasserintensiv. Ein Recycling ist möglich, aber ebenfalls energieintensiv.
- Mikroplastik und Mikrofasern, die sich beim Waschen aus Polyester-Textilien lösen und so ins Abwasser und Meer gelangen.[9][10]
Weblinks
Einzelnachweise
- ↑ Wolfgang Kaiser: Kunststoffchemie für Ingenieure, 3. Auflage, Carl Hanser, München, 2011, S. 331.
- ↑ Charles Carraher: Polyesters, Chemistry explained.
- ↑ Artikel Whinfield, Lexikon bedeutender Chemiker, Harri Deutsch, 1989.
- ↑ Oskar Nuyken, Heidi Samarian, Ilse Wurdack: Polymere in der Medizintechnik. In: ChemgaPedia. ChemgaPedia der Wiley Information Services GmbH, S. 8, abgerufen am 30. August 2016.
- ↑ Indra K. Varma, Ann-Christine Albertsson, Ritimoni Rajkhowa, Rajiv K. Srivastava: Enzyme catalyzed synthesis of polyesters. In: Progress in Polymer Science. Band 30, Nr. 10, S. 949–981, doi:10.1016/j.progpolymsci.2005.06.010 (elsevier.com [abgerufen am 25. Januar 2018]).
- ↑ Fachuni Chemie Berlin – Kunststofftabelle (Polykondensate/Polyester).
- ↑ Hinweis auf Grisuten als Warenzeichen der DDR.
- ↑ Lexikoneintrag Lacke, Internetpräsenz der Zeitschrift 'Spektrum der Wissenschaft'.
- ↑ Melanie Klawitter: Polyester: Geht so nachhaltiges Plastik? Utopia.de, 6. Februar 2022.
- ↑ Mikrofasern aus Kleidungsstücken belasten die Ozeane. Greenpeace, Februar 2017.