3-Chlor-4-methylanilin
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
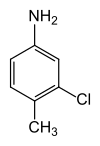
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 3-Chlor-4-methylanilin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H8ClN | |||||||||||||||
| Kurzbeschreibung |
bei Raumtemperatur langsam schmelzender Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 141,60 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig oder fest[1] | |||||||||||||||
| Dichte |
1,17 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
237–238 °C[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,584 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
3-Chlor-4-methylanilin ist eine chemische Verbindung aus der Gruppe der Aminobenzole und Monochloraniline. Das Hydrochlorid der Verbindung ist aufgrund der hohen Giftigkeit für Vögel auch unter dem Namen Starlicid bekannt.[4]
Gewinnung und Darstellung
3-Chlor-4-methylanilin kann durch Chlorierung von p-Nitrotoluol und anschließende katalytische Reduktion an sulfidierten Palladium/Aktivkohle-Kontakten gewonnen werden.[5]
Eigenschaften
3-Chlor-4-methylanilin ist ein brennbarer, schwer entzündbarer, bei Raumtemperatur langsam schmelzender Feststoff, der schwer löslich in Wasser ist. Bei Temperaturen über dem Schmelzpunkt gelbbraune Flüssigkeit. Ein verunreinigtes Produkt kann auch bei Raumtemperatur flüssig sein. Die Zersetzungstemperatur der Verbindung liegt über 500 °C, wobei bei der Zersetzung unter anderem Chlorwasserstoff entsteht.[1] Von der Verbindung sind zwei stabile und eine metastabile Phase bekannt.[6]
Verwendung
3-Chlor-4-methylanilin wird zur Herstellung von 2-Chlor-4-cyanotoluol durch Sandmeyer-Reaktion mit Kupfer(I)-cyanid verwendet.[3] Es kann auch als Zwischenprodukt zur Herstellung von anderen chemischen Verbindungen, wie dem Herbizid Chlortoluron, eingesetzt werden.[5] Das Hydrochlorid von 3-Chlor-4-methylanilin ist seit 1967 in den USA zur Vogelbekämpfung zugelassen.[4]
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu 3-Chlor-4-methylanilin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ David R. Lide: CRC Handbook of Chemistry and Physics A Ready-reference Book of Chemical and Physical Data. CRC Press, 1995, ISBN 978-0-8493-0595-5, S. 114 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Datenblatt 2-Chloro-4-aminotoluene, 98% bei Sigma-Aldrich, abgerufen am 21. November 2018 (PDF).
- ↑ a b EPA: Starlicide (3-chloro-p-toluidine hydrochloride)
- ↑ a b Heinz-Gerhard Franck, Jürgen W. Stadelhofer: Industrielle Aromatenchemie Rohstoffe · Verfahren · Produkte. Springer-Verlag, 2013, ISBN 978-3-662-07875-4, S. 492 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ S. K. Roy, B. Amitha, J. Uchil: Study of polymorphism and torsional motions in 3-chloro-4-methylaniline using Cl NQR (nuclear quadrupole resonance). In: Canadian Journal of Physics. 70, 1992, S. 119, doi:10.1139/p92-015.

