β-Galactosidase
| β-Galactosidase | ||
|---|---|---|
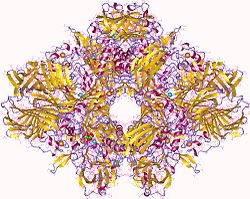
| ||
| Beta-galactosidase tetramer, E.Coli nach PDB 3MV0 | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 649 Aminosäuren | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Namen | GLB1 ; EBP; ELNR1; S-Gal | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | A16AB04 | |
| DrugBank | DB00103 | |
| Enzymklassifikation | ||
| EC, Kategorie | 3.2.1.23, Glycosidase | |
| Reaktionsart | Hydrolyse endständiger β-D-Galactose-Reste in β-D-Galactosiden | |
| Substrat | β-D-Galactoside | |
| Produkte | β-D-Galactose | |
| Vorkommen | ||
| Homologie-Familie | Galactosidase 3 | |
| Übergeordnetes Taxon | Lebewesen | |
β-Galactosidasen (auch β-Galaktosidasen) sind Enzyme, die endständige, glycosidisch gebundene β-D-Galactose von Biomolekülen (z. B. Gangliosiden, Glycoproteinen und Glycosaminoglycanen) hydrolytisch abspalten. Sie kommen in allen Lebewesen vor, wo sie unterschiedlichen Stellenwert im Stoffwechsel haben. Bakterielle β-Galactosidase wird im Labor verwendet. Außer der bakteriellen Lactase, die ebenfalls eine β-Galactosidase ist, gibt es auch eine menschliche Lactase, die nicht zu EC 3.2.1.23 gerechnet wird. Das menschliche Enzym wird vom GLB1-Gen in zwei Spleißvarianten codiert, die in allen Zellen sowohl in den Lysosomen als auch im Zytoplasma vorkommen. Mutationen im GLB1-Gen können zu verschiedenen Typen der Gangliosidose und zu Typ 4B der Mucopolysaccharidose führen.[1]
Funktion
Als Exoglycosidasen katalysieren sie die Hydrolyse der glycosidischen Bindung von β-Galactopyranosiden. Dabei entsteht das Monosaccharid Galactose. β-Galactosidasen sind je nach Aufgabe und Organismus unterschiedlich spezifisch; so können einige von ihnen auch α-L-Arabinopyranoside hydrolysieren. Die β-Galactosidase aus dem Darmbakterium Escherichia coli hydrolysiert das Disaccharid Lactose zu D-Galactose und D-Glucose und produziert zusätzlich das Isomer Allolactose, den natürlichen Induktor des lac-Operons, durch intramolekulare Umlagerung.[2] Dabei wird die β1→4-glycosidische Bindung der Lactose in die β1→6-glycosidische Bindung der Allolactose überführt. In einer weiteren Reaktion wird die gebildete Allolactose durch die β-Galactosidase wie Lactose zu D-Glucose und D-Galactose hydrolysiert.
Verwendung
In der Mikro- und Molekularbiologie wird das aus dem gramnegativen Bakterium Escherichia coli stammende Gen für die β-Galactosidase, genannt lacZ, als Reportergen verwendet. In mit Gentechnik veränderten Bakterien (z. B. Blau-Weiß-Selektion von Kolonien), Hefen (z. B. Hefe-Zwei-Hybrid-System) oder auch höheren Organismen (z. B. Knockout-Maus) zeigt die Hydrolyse von X-Gal (5-Brom-4-chlor-3-indoxyl-β-D-galactopyranosid) zu Galactose und einem blauen, wasserunlöslichen Indigo-Farbstoff die Genexpression von lacZ an.
Die enzymatische Aktivität der β-Galactosidase wird mit Hilfe der hydrolytischen Spaltung von ONPG (o-Nitrophenyl-β-D-galactopyranosid) gemessen. Industriell wird β-Galactosidase intensiv in der Milchindustrie eingesetzt, so zum Beispiel bei der Produktion von lactosefreier Milch oder bei der Behandlung von Molke.
Klassifikation
β-Galactosidasen bilden Familie 35 in der Klassifikation der Glycosidasen nach Henrissat.[3]
Einzelnachweise
- ↑ UniProt P16278
- ↑ Robert W Wheatley, Summie Lo, Larisa J. Jancewicz, Megan L. Dugdale, Reuben E Huber: Structural explanation for allolactose (lac operon inducer) synthesis by lacZ β-galactosidase and the evolutionary relationship between allolactose synthesis and the lac repressor. In: Journal of Biological Chemistry, Band 288, Ausgabe 18, S. 12993-3005, 2013, doi:10.1074/jbc.M113.455436.
- ↑ Bernard Henrissat: Glycosyl hydrolase families: classification and list of entries.