Bromaceton
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
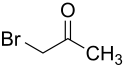
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Bromaceton | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C3H5BrO | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 136,97 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Dichte |
1,63 g·cm−3[1] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
136,5 °C[1] | ||||||||||||
| Dampfdruck | |||||||||||||
| Löslichkeit |
sehr schwer in Wasser[1] | ||||||||||||
| Brechungsindex |
1,4697 (15 °C)[2] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||
Bromaceton ist eine farblose, stechend riechende Flüssigkeit, die früher als Augenreizstoff in Tränengasen verwendet wurde.[3] In dieser Funktion wurde es zunächst zeitweise durch ω-Chloracetophenon (CN) abgelöst, heute wird dies weitgehend durch 2-Chlorbenzyliden-malonsäuredinitril (CS) ersetzt.
Geschichte
Brom- und Chloraceton gehörten zu den ersten im Krieg eingesetzten Kampfstoffen. Im Ersten Weltkrieg wurden sie unter Bezeichnung Weißkreuz vom Deutschen Heer eingesetzt. Auch heute noch finden sie zum Teil bei der Polizei als Tränengas Verwendung.
Herstellung
Die Herstellung von Bromaceton ist sehr einfach: Brom und Aceton reagieren bereits bei Zimmertemperatur unter Selbsterhitzung zu Bromaceton und Bromwasserstoff. Das aufkochende Aceton wirkt als Treibsatz für das Tränengas.
Eigenschaften
Bromaceton greift in erster Linie die Augen, aber auch die oberen Schleimhäute (Nase und Rachen) an. Die Symptome treten sofort auf und verschwinden nach Ende der Einwirkung schnell wieder.
α-Halogencarbonylverbindungen wirken korrosiv auf Metalle (Eisen, Messing).
Siehe auch
Einzelnachweise
- ↑ a b c d e f Eintrag zu Bromaceton in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-56.
- ↑ Wolfgang Legrum: Riechstoffe, zwischen Gestank und Duft, Vieweg + Teubner Verlag (2011) S. 74–75, ISBN 978-3-8348-1245-2.


