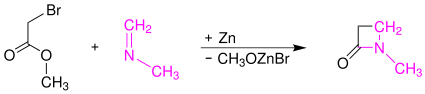Gilman-Speeter-Kondensation
Die Gilman-Speeter-Kondensation ist eine Namensreaktion aus dem Bereich der Organischen Chemie, die 1943 erstmals durch die US-amerikanischen Chemiker Henry Gilman (1893–1986) und Merrill E. Speeter publiziert wurde.[1] Sie ist eine effiziente Synthese eines β-Lactams aus einem Reformatsky-Reagenz und einem Imin.[2]
Übersicht
Das halogenidsubstituierte, in diesem Fall bromidsubstituierte, Reformatsky-Reagenz wird mit einem Imin, hier N-Methylmethanimin, zu einem β-Lactam, in diesem Fall 1-Methylazetidin-2-on, umgesetzt:
Mit der Gilman-Speeter-Kondensation lassen sich durch den Einsatz entsprechender Imine auch 3-alkyl-4-alkenylsubstituierte β-Lactame synthetisieren.
Reaktionsmechanismus
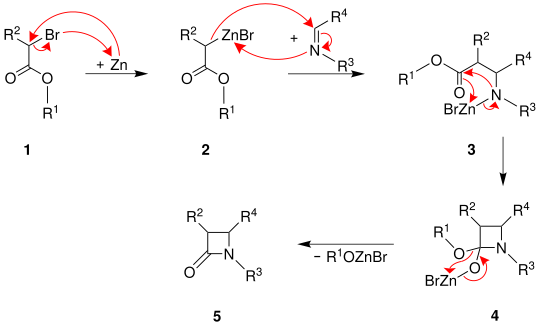
Ein Vorschlag für den Reaktionsmechanismus:[3]
Aus dem α-Bromester 1 wird durch Addition eines Zinkatoms das (Reformatsky-Reagenz) 2 synthetisiert. Anschließend wird das Zinkorganyl 2 an die C=N-Doppelbindung des Imins addiert. Das Intermediat 3 cyclisiert zu dem Heterocyclus 4 der zu dem β-Lactam 5 weiterreagiert.[3] Dabei haben die Reste folgende Bedeutung: R1 = Alkylrest; R2 = H oder Alkylrest; R3 = Alkyl- oder Arylrest; R4 = H, Alkyl- oder Arylrest.