Hafniumnitrid
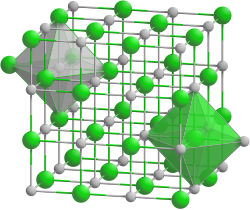
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Hf3+ _ N3− | ||||||||||
| Allgemeines | ||||||||||
| Name | Hafniumnitrid | |||||||||
| Andere Namen |
| |||||||||
| Verhältnisformel | HfN | |||||||||
| Kurzbeschreibung |
dunkelgrauer bis brauner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 192,50 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
11,7 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[3] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Hafniumnitrid ist eine anorganische chemische Verbindung des Hafniums aus der Gruppe der Nitride.
Gewinnung und Darstellung
Hafniummnitrid kann nach den gleichen Verfahren wie Titannitrid dargestellt werden.[5]
- So erhält man Hafniumnitrid bei der Synthese aus den Elementen bei 1400 °C bis 1500 °C.[5]
- Bei der Herstellung von Hafniumnitrid aus Hafnium(IV)-chlorid durch das Aufwachsverfahren wird bei Gegenwart von Wasserstoff (H2 + N2 oder Ammoniak) eine tiefere Temperatur (2000 bis 2400 °C) benötigt als in reinem Stickstoff (2900 °C). Im letzteren Fall erfolgt die Abscheidung bedeutend langsamer als bei Anwesenheit von Wasserstoff.[5]
- Unter Hochdruckbedingungen bildet sich bei Ammonolyse oder Reaktion von Hafniumnitrid mit Stickstoff ein Hafniumnitrid Hf3N4 vom kubischen Th3P4-Typ mit der Raumgruppe I43d.[6]
Eigenschaften
Hafniumnitrid ist ein dunkelgrauer bis gelbbrauner geruchloser Feststoff. Er ist elektrisch leitend und hat eine kubische Kristallstruktur[1] vom Natriumchlorid-Typ mit der Raumgruppe Fm3m (Nr. 225).[7][6] Durch Leerstellen in der Gitterstruktur beträgt die reale Dichte von Hafniumnitrid nur 11,70 g·cm−3 anstelle der auf Basis von Gitterstrukturanalysen mit Röntgenverfahren bestimmten 13,39 g·cm−3.[2] Es ist ein sehr hartes und beständiges Material[8] und hat eine Vickershärte von 46 GPa[9].
Verwendung
Hafniumnitrid wird als Sputtermaterial zur Erhöhung der Stabilität von Dioden, Transistoren und elektronischen Schaltkreisen verwendet.[8] Es wird auch als Beschichtungsmaterial von Schneidwerkzeugen verwendet,[10] da es der stabilste Hartstoff mit hoher Schmelztemperatur ist.[11]
Einzelnachweise
- ↑ a b c Der BibISBN-Eintrag [[Vorlage:BibISBN/Skriptfehler: Das Modul gab einen nil-Wert zurück. Es wird angenommen, dass eine Tabelle zum Export zurückgegeben wird.]] ist nicht vorhanden. Bitte prüfe die ISBN und lege ggf. einen [{{fullurl:Vorlage:bibISBN/Skriptfehler: Das Modul gab einen nil-Wert zurück. Es wird angenommen, dass eine Tabelle zum Export zurückgegeben wird.|action=edit§ion=new&preload=Vorlage%3ABibISBN%2FVorlage&nosummary=1}} <span title="Vorlage:bibISBN/Skriptfehler: Das Modul gab einen nil-Wert zurück. Es wird angenommen, dass eine Tabelle zum Export zurückgegeben wird. (Seite nicht vorhanden)">neuen Eintrag] an..
- ↑ a b M. E. Straumanis, C. A. Faunce: Der unvollkommene Aufbau des Hafniumnitrids und das Bindungsproblem. In: Zeitschrift für anorganische und allgemeine Chemie. 353, 1967, S. 329–336, Modul:Vorlage:Handle * library URIutil invalid.
- ↑ READE: Hafnium Nitride Powder (HfN) (Memento des Originals vom 6. August 2013 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Datenblatt Hafniumnitrid −325 mesh, 99% bei Sigma-Aldrich, abgerufen am 20. Juli 2022 (PDF).
- ↑ a b c Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 1379.
- ↑ a b Dzivenko, Dmytro: High-pressure synthesis, structure and properties of cubic zirconium(IV)- and hafnium(IV) nitrides. Dissertation (2009),
- ↑ Werner Martienssen, Hans Warlimont: Springer Handbook of Condensed Matter and Materials Data. Springer, 2005, ISBN 9783540304371, S. 468 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis US, 2011, ISBN 1439814627, S. 194 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Derya Deniz: Texture evolution in metal nitride (aluminum nitride, titanium nitride, hafnium nitride) thin films prepared by off-normal incidence reactive magnetron sputtering. ProQuest, 2008, ISBN 9781109037821, S. 6 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Serope Kalpakjian, Steven R. Schmid, Ewald Werner: Werkstofftechnik. Pearson Deutschland GmbH, 2011, ISBN 978386894006-0, S. 634 (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ Hmt, Hmt, H. M T. Bangalore: Production Technology. Tata McGraw-Hill Education, 2001, ISBN 9780070964433, S. 41 (eingeschränkte Vorschau in der Google-Buchsuche).
