Kaliumperoxomonosulfat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
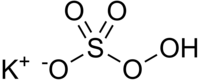
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kaliumperoxomonosulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | KHSO5 | |||||||||||||||
| Kurzbeschreibung |
weißer geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 152,16 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
2,18 g·cm−3 (Monohydrat)[2] | |||||||||||||||
| Schmelzpunkt |
109 °C[3] | |||||||||||||||
| Löslichkeit |
löslich in Wasser[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Kaliumperoxomonosulfat ist eine anorganische chemische Verbindung des Kaliums aus der Gruppe der Sulfate und das Kaliumsalz der Peroxomonoschwefelsäure.
Gewinnung und Darstellung
Kaliumperoxomonosulfat kann durch Reaktion von Kaliumcarbonat oder Kaliumhydroxid mit Peroxomonoschwefelsäure gewonnen werden.[3]
Kaliumperoxomonosulfat-Monohydrat kann aus dem Tripelsalz oder durch Hydrolyse von Kaliumperoxodisulfat gewonnen werden.[5][2] Das Anhydrat kann daraus durch Trocknung im Vakuum gewonnen werden.[6]
Eigenschaften
Von Kaliumperoxomonosulfat existiert auch ein Monohydrat mit monokliner Kristallstruktur und der Raumgruppe C2/c (Raumgruppen-Nr. 15).[3][2]
Verwendung
Kaliumperoxomonosulfat wird als Oxidationsmittel bei der chemischen Synthese,[7] als Desinfektionsmittel in Schwimmbädern, der Medizin und in der Wasseraufbereitung verwendet.[8]
Tripelsalz
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| Name |
Tripelsalz | |||||||
| CAS-Nummer | ||||||||
| EG-Nummer |
274-778-7 | |||||||
| ECHA-InfoCard | ||||||||
| ||||||||
Als Tripelsalz wird eine Mischung aus Kaliumperoxomonosulfat, Kaliumhydrogensulfat und Kaliumsulfat (2KHSO5·KHSO4·K2SO4) bezeichnet.
Hierbei handelt es sich um einen kristallinen weißen geruchlosen Feststoff, der leicht löslich in Wasser (256 g·l−1 bei 20 °C) ist. Er zersetzt sich bei Erhitzung über ca. 90 °C. Seine wässrige Lösung reagiert stark sauer. Die Dichte liegt bei 1,1–1,2 g·cm−3, der Schmelzpunkt bei 90 °C (Zersetzung).[9]
Das Tripelsalz wird zur Halogenierung von α,β-ungesättigten Carbonylverbindungen und zur katalytischen Erzeugung von hypervalenten Iodverbindungen für Alkoholoxidation und für Synthese von Oxaziridinen und Dioxiranen wie Dimethyldioxiran verwendet.[10][11] Dies ist die Basis der Shi-Epoxidierung.[12]
Weiterhin wird das Tripelsalz als Bleich- und Reinigungszusatz für Textilien und Zahnprothesen sowie als Ätzmittel zur Oberflächenbehandlung verwendet.[13] Es dient auch zur Schrumpffestausrüstung der Wolle.[14]
Handelsnamen des Tripelsalzes sind „Oxone“ oder „Caroat“.
Einzelnachweise
- ↑ a b Andreas Agster: Färberei und textilchemische Untersuchungen. Springer Berlin Heidelberg, S. 131 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c E. O. Schlemper, R. C. Thompson, C. K. Fair, F. K. Ross, E. H. Appelman, L. J. Basile: Structure, deformation density and atomic charges in potassium hydrogenperoxomonosulfate monohydrate, KHSO5·H2O. In: Acta Crystallographica Section C: Crystal Structure Communications. Band 40, Nr. 11, 1984, ISSN 0108-2701, S. 1781–1785, doi:10.1107/S0108270184009537 (iucr.org).
- ↑ a b c d Jane E. Macintyre: Dictionary of Inorganic Compounds. CRC Press, 1992, ISBN 978-0-412-30120-9, S. 3535 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Travis, B., Ciaramitaro, B., Borhan, B. (2002): Preparation of Purified KHSO5·H2O and nBu4NHSO5 from Oxone by Simple and Efficient Methods. Eur. J. Org. Chem., 2002: 3429–3434, doi:10.1002/1099-0690(200210)2002:20<3429::AID-EJOC3429>3.0.CO;2-D
- ↑ Evan H. Appelman, Louis J. Basile, Hyunyong Kim, John R. Ferraro: Molecular vibrational spectra of potassium peroxymonosulfate, KHSO5 and KHSO5 · H2O, and of the aqueous peroxymonosulfate ion. In: Spectrochimica Acta Part A: Molecular Spectroscopy. Band 41, Nr. 11, 1985, ISSN 0584-8539, S. 1295–1300, doi:10.1016/0584-8539(85)80237-3.
- ↑ Albert Matlack: Introduction to Green Chemistry, Second Edition. CRC Press, 2010, ISBN 978-1-4398-8211-5, S. 86 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Johann Mutschmann, Fritz Stimmelmayr: Taschenbuch der Wasserversorgung. Springer-Verlag, 2013, ISBN 978-3-663-12397-2, S. 191 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Eintrag zu Pentakaliumbis(peroxymonosulfat)bis(sulfat) in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- ↑ F.von Rheinbaben, M.H. Wolff: Handbuch der viruswirksamen Desinfektion. Springer-Verlag, 2013, ISBN 978-3-642-56394-2, S. 127 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Oxone, monopersulfate bei AlfaAesar, abgerufen am 15. Juli 2016 (PDF) (JavaScript erforderlich).
- ↑ Michael Frohn, Yian Shi: Chiral Ketone-Catalyzed Asymmetric Epoxidation of Olefins. In: Synthesis. 2000, S. 1979, doi:10.1055/s-2000-8715.
- ↑ HELM AG: Kaliumperoxomonosulfat (Memento vom 15. August 2016 im Internet Archive), abgerufen: 15. Juli 2016.
- ↑ Eintrag zu Kaliumhydrogenperoxomonosulfat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 19. April 2017.

