Kupfer(II)-tetrafluoroborat
aus Wikipedia, der freien Enzyklopädie
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
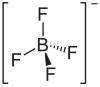
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Kupfer(II)-tetrafluoroborat | ||||||||||||
| Summenformel | Cu[BF4]2 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 237,16 g·mol−1 (wasserfrei) | ||||||||||||
| Aggregatzustand |
fest (Hydrat)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Kupfer(II)-tetrafluoroborat ist eine anorganische Verbindung. Es handelt sich um ein Salz des Kupfers in der Oxidationsstufe +II mit der Tetrafluorborsäure.
Darstellung
Kupfer(II)-tetrafluoroborat lässt sich durch die Umsetzung von Kupfer(II)-oxid, -carbonat oder -hydroxid mit wässriger Tetrafluorborsäure darstellen.[2]
- Fehler beim Parsen (Konvertierungsfehler. Der Server („https://wikimedia.org/api/rest_“) hat berichtet: „Cannot get mml. Server problem.“): {\displaystyle \mathrm {CuO\ +\ 2\ HBF_{4}\longrightarrow \ Cu[BF_{4}]_{2}\ +\ H_{2}O} }
Eigenschaften
Kupfer(II)-tetrafluoroborat kristallisiert mit einer unbestimmten Zahl an Kristallwasser-Molekülen. Es zersetzt sich an feuchter Luft oder in Gegenwart von Wasser.[1]
Verwendung
Das Tetrafluoroboratanion zählt zu den schwach koordinierendes Anionen, weshalb es leicht durch andere Liganden ausgetauscht werden kann. Aus diesem Grund kann Kupfer(II)-tetrafluoroborat zur Synthese von Kupferkomplexen eingesetzt werden.
Einzelnachweise
- ↑ a b c d Datenblatt Copper(II) tetrafluoroborate hydrate bei Sigma-Aldrich, abgerufen am 4. Februar 2019 (PDF).
- ↑ Eintrag zu Fluoridoborate. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Dezember 2014.