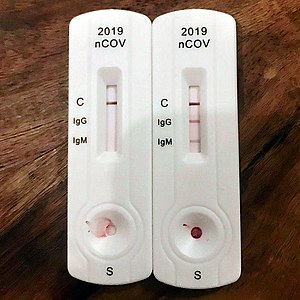
Lateral-Flow-Test
Der Lateral-Flow-Test, auch Lateral-Flow-Assay (englisch für „seitlicher Flusstest“) ist eine biochemische Methode zum qualitativen Nachweis von Stoffen (z. B. Antigenen) mit Antikörpern.[1][2][3] Der lateral flow test ist eine Kombination aus einer Dünnschichtchromatographie und einer Immunfärbung. Aufgrund des im Vergleich zu anderen Immunassays geringeren Geräteaufwands werden lateral flow tests oftmals in Form von Teststreifen verwendet,[4] z. B. Schwangerschaftsteststreifen, Drogenteststreifen, Influenza- und Corona-Schnelltests oder Allergenschnelltests.
Prinzip
Die zu untersuchende Probe wird auf den Probenbereich (englisch sample pad) auf einem Teststreifen aus porösem Papier oder gesintertem Polymer aufgetragen. Die Probe beginnt nach Zugabe des Laufmittels mit der Ausbreitung über den Teststreifen aufgrund von Kapillarkräften (Dünnschichtchromatographie). Die Probe wandert mit der Flüssigkeit zu einem Bereich, wo sich getrocknete Immunkonjugate mit Salzen und Kohlenhydraten befinden (englisch conjugate pad). Die Flüssigkeit löst das Immunkonjugat, wodurch es an die nachzuweisenden Moleküle (das Antigen) in der Probe binden kann, sofern vorhanden. Die Flüssigkeit wandert weiter in den Kapillarbereich (englisch capture pad), wo in einem kleinen Abschnitt ein Antikörper immobilisiert wurde, der an einer anderen Stelle auf der Oberfläche des nachzuweisenden Moleküls bindet und dieses dadurch in diesem Bereich bindet und anreichert, während die Flüssigkeit weiterwandert. Durch die Anreicherung des nachzuweisenden Moleküls entsteht anhand des gebundenen Immunkonjugats je nach Immunkonjugat z. B. eine Färbung, eine Fluoreszenzfärbung oder eine magnetische Markierung. Auf dem Teststreifen befindet sich ein Bereich für eine Positivkontrolle, die eine prinzipielle Funktionsfähigkeit des Tests anzeigt (im Bild mit 'C' für engl. control markiert). Gelegentlich wird nebenbei ein zweiter Teststreifen verwendet, der als Negativkontrolle mit Kontrollflüssigkeit verwendet wird und falsch-positive Ergebnisse ausschließt.
Lateral Flow Tests können sowohl qualitativ als auch quantitativ eingesetzt werden. Ein qualitativer Test untersucht nur die Probe auf die An- oder Abwesenheit eines gesuchten Analyten, während ein quantitativer lateral flow Test auch die Konzentration des gesuchten Analyten angeben kann. Dies geschieht über die Interpretation der Bandenintensität des Analyten mit Hilfe eines optischen Lesegerätes. Das Lesegerät vergleicht hierbei die Bandenintensität mit einer hinterlegten Standardkurve und kann darüber eine Konzentration für den Analyten ausgeben. Quantitative Tests können sowohl über sichtbare Färbung der Testbanden (z.b. Goldkonjugat) als auch über Fluoreszenzmarkierte Färbung der Testbanden ausgewertet werden.
Weblinks
- Welche Covid-19 Schnelltests gibt es und wie funktionieren sie? auf science.lu
- Funktionsweise eines Lateral-Flow-Tests auf der Webseite der Fassisi GmbH
Einzelnachweise
- ↑ L. Kulinsky, Z. Noroozi, M. Madou: Present technology and future trends in point-of-care microfluidic diagnostics. In: Methods in Molecular Biology (Clifton, N.J.). Band 949, 2013, S. 3–23, ISSN 1940-6029. doi:10.1007/978-1-62703-134-9_1. PMID 23329432.
- ↑ C. Rozand: Paper-based analytical devices for point-of-care infectious disease testing. In: European Journal of Clinical Microbiology & Infectious Diseases. Band 33, Nummer 2, Februar 2014, S. 147–156, ISSN 1435-4373. doi:10.1007/s10096-013-1945-2. PMID 23982665.
- ↑ A. St John, C. P. Price: Existing and Emerging Technologies for Point-of-Care Testing. In: Clinical Biochemist Reviews. Band 35, Nummer 3, August 2014, S. 155–167, ISSN 0159-8090. PMID 25336761. PMC 4204237 (freier Volltext).
- ↑ A. K. Yetisen, M. S. Akram, C. R. Lowe: Paper-based microfluidic point-of-care diagnostic devices. In: Lab on a Chip. Band 13, Nummer 12, Juni 2013, S. 2210–2251, ISSN 1473-0189. doi:10.1039/c3lc50169h. PMID 23652632.