Lutetium(III)-chlorid
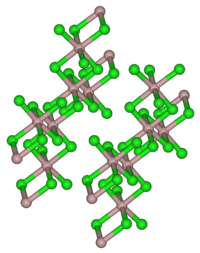
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| _ Lu3+ _ Cl− | |||||||
| Raumgruppe |
C2/m (Nr. 12) | ||||||
| Allgemeines | |||||||
| Name | Lutetium(III)-chlorid | ||||||
| Andere Namen | |||||||
| Verhältnisformel | LuCl3 | ||||||
| Kurzbeschreibung | |||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | |||||||
| Aggregatzustand |
fest[3] | ||||||
| Dichte |
3,98 g·cm−3[2] | ||||||
| Schmelzpunkt | |||||||
| Siedepunkt |
1480 °C[4] | ||||||
| Löslichkeit |
löslich in Wasser[2] | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Toxikologische Daten | |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Lutetium(III)-chlorid ist eine chemische Verbindung aus der Gruppe der Chloride.
Gewinnung und Darstellung
Lutetium(III)-chlorid kann durch Reaktion von Lutetium(III)-oxid oder Lutetium(III)-carbonat und Ammoniumchlorid gewonnen werden.[4]
Das Hexahydrat entsteht durch Reaktion von Lutetium mit Salzsäure. Durch Reaktion mit Thionylchlorid kann dieses zur Anhydratform umgesetzt werden.[4]
Lutetium(III)-chlorid kann auch direkt aus den Elementen Lutetium und Chlor synthetisiert werden.[6]
Eigenschaften
Lutetium(III)-chlorid und sein Hexahydrat sind farblose Feststoffe.[7] Beide sind löslich in Wasser.[2] Lutetium(III)-chlorid besitzt eine monokline Kristallstruktur mit der Raumgruppe C2/m (Nr. 12) entsprechend der von Aluminium(III)-chlorid.[4][2]
Verwendung
Lutetium(III)-chlorid kann zur Herstellung von reinem Lutetium verwendet werden.[8]
Einzelnachweise
- ↑ Eintrag zu LUTETIUM CHLORIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 18. September 2021.
- ↑ a b c d e Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 2007, ISBN 978-3-540-60035-0, S. 544 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e Datenblatt Lutetium(III) chloride, anhydrous, powder, 99.9% trace metals basis bei Sigma-Aldrich, abgerufen am 30. April 2012 (PDF).
- ↑ a b c d e Georg Brauer: Handbuch der Präparativen Anorganischen Chemie, Band 2, ISBN 3-432-87813-3, S. 897.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Properties of the Elements and Inorganic Compounds, S. 4-72.
- ↑ Webelements: Lutetium
- ↑ Datenblatt Lutetium(III) chloride hexahydrate (99.9%-Lu) (PDF) bei Strem, abgerufen am 25. Dezember 2012.
- ↑ Patnaik Pradyot: Handbook of Inorganic Chemicals. McGraw-Hill Professional, 2002, ISBN 978-0-07-049439-8.




