Pyridiniumtribromid
aus Wikipedia, der freien Enzyklopädie
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
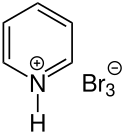
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Pyridiniumtribromid | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C5H6Br3N | ||||||||||||
| Kurzbeschreibung |
roter geruchloser Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 319,82 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Löslichkeit | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Pyridiniumtribromid ist eine chemische Verbindung des Broms aus der Gruppe der Pyridiniumverbindungen.
Gewinnung und Darstellung
Pyridiniumtribromid kann durch Reaktion von Pyridiniumhydrobromid mit Brom oder Thionylbromid gewonnen werden.[4]
Eigenschaften
Pyridiniumtribromid ist ein kristalliner roter geruchloser Feststoff, der praktisch unlöslich in Wasser ist.[3][1]
Verwendung
Pyridiniumtribromid wird als Bromierungsreagenz von Ketonen, Phenolen und Ethern verwendet.[3] Es hat dabei mehrere Vorteile gegenüber elementarem Brom, wie etwa das sehr präzise Abwiegen bei Reaktionen im kleinen Maßstab. Ein Beispiel für die Anwendung ist die Bromierung des 3-Ketosteroids 1 zum 2,4-Dibromcholestanon (2):[5][6][7]
Einzelnachweise
- ↑ a b Datenblatt Pyridiniumbromidperbromid bei Merck, abgerufen am 13. August 2017.
- ↑ a b c d Datenblatt Pyridinium tribromide, technical grade, 90% bei Sigma-Aldrich, abgerufen am 13. August 2017 (PDF).
- ↑ a b c d Datenblatt Pyridine hydrobromide perbromide, tech. 90% bei AlfaAesar, abgerufen am 13. August 2017 (PDF) (JavaScript erforderlich).
- ↑ Houben-Weyl Methods of Organic Chemistry Vol. V/4, 4th Edition: Bromine and Iodine Compounds. Georg Thieme Verlag, 2014, ISBN 978-3-13-180014-5, S. 35 (books.google.de).
- ↑ Jürgen Falbe, Manfred Regitz: Römpp-Chemie-Lexikon. Thieme, Stuttgart 1992, ISBN 3-13-735009-3, S. 3696–3697.
- ↑ Carl Djerassi, Caesar R. Scholz: Brominations with Pyridine Hydrobromide Perbromide. In: Journal of the American Chemical Society. 70, Nr. 1, Januar 1948, S. 417–418. doi:10.1021/ja01181a508.
- ↑ Jonathan Clayden, Nick Greeves, Stuart Warren: Organische Chemie. 2. Auflage. Springer Spektrum, Berlin Heidelberg 2013, ISBN 978-3-642-34715-3, S. 802–804.

