Rubidiumchlorid
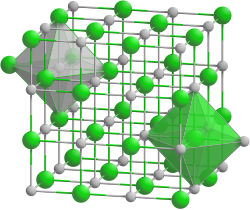
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Rb+ _ Cl− | ||||||||||||||||
| Kristallsystem |
kubisch | |||||||||||||||
| Raumgruppe |
Fm3m (Nr. 225) | |||||||||||||||
| Koordinationszahlen |
Rb[6], Cl[6] | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Rubidiumchlorid | |||||||||||||||
| Verhältnisformel | RbCl | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 120,92 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,76 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
1390 °C[1] | |||||||||||||||
| Löslichkeit |
gut in Wasser (910 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Brechungsindex |
1,493[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Rubidiumchlorid ist eine weiße, kristalline Verbindung aus den Elementen Rubidium und Chlor mit der Formel RbCl. Sie ist im Handel auch als feines Pulver erhältlich. Rubidiumchlorid kristallisiert im kubischen Natriumchlorid-Strukturtyp.
Gewinnung und Darstellung
Rubidiumchlorid kann durch Neutralisation von wässriger Rubidiumhydroxid-Lösung durch Salzsäure gewonnen werden:
Eigenschaften
| Löslichkeit von RbCl in verschiedenen Alkoholen[4] (angegeben in g/l bei 25 °C) | |
| Methanol | 14,1 |
| Ethanol | 0,78 |
| n-Propanol | 0,15 |
| Amylalkohol | 0,025 |
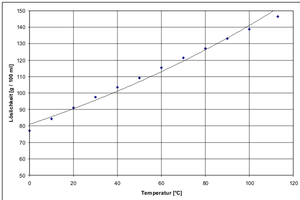
Rubidiumchlorid ist hygroskopisch. Der Schmelzpunkt liegt bei 718 °C. Die Wasserlöslichkeit nimmt mit steigender Temperatur zu.[3] Der Brechungsindex der Kristalle beträgt nD = 1.4936, der Gitterparameter a = 658,1 pm, in der Elementarzelle befinden sich vier Formeleinheiten.[5]
Die Löslichkeit in Aceton beträgt 0,0021 g/kg bei 18 °C, sowie 0,0024 g/kg bei 37 °C.[4] Die Löslichkeit in verschiedenen Alkoholen ist in der Tabelle angegeben.
Die Standardbildungsenthalpie von Rubidiumchlorid beträgt ΔfH0298 = −430,86 kJ·mol−1,[6] die Freie Standardbildungsenthalpie ΔG0298 = −405,3 kJ·mol−1.[6]
Rubidiumchlorid bildet mit verschiedenen Metallchloriden gut kristallisierende Doppelsalze.[7]
Verwendung
Rubidiumhalogenide wie Rubidiumchlorid, Rubidiumbromid und Rubidiumiodid werden therapeutisch als Schmerz- und Beruhigungsmittel sowie als Antidepressivum eingesetzt.[8] 82Rb-Rubidiumchlorid wird als Tracer zur Myokardszintigrafie verwendet.[9]
Weblinks
Einzelnachweise
- ↑ a b c d e f g h Datenblatt Rubidiumchlorid bei Merck, abgerufen am 19. Januar 2011.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Index of Refraction of Inorganic Crystals, S. 10-247.
- ↑ a b R. Abegg, F. Auerbach, I. Koppel: "Handbuch der anorganischen Chemie", Verlag S. Hirzel, 1908, 2. Band, 1. Teil, S. 426ff. Volltext
- ↑ a b Aterton Seidell: "Solubilities Of Organic Compounds Vol - I", S. 1429. Volltext
- ↑ Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 686 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b R. E. Dickerson, H. B. Gray, H.-W. Sichting, M. Y. Darensbourg: "Prinzipien der Chemie", Verlag Walter de Gruyter 1988, ISBN 9783110099690, S. 976. (eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ R. Godeffroy: "Einige neue Salze und Reactionen des Caesiums und Rubidiums" in Berichte der deutschen chemischen Gesellschaft 1875, 8(1), S. 9–11. doi:10.1002/cber.18750080104 Volltext
- ↑ H. Erdmann: Lehrbuch der anorganischen Chemie, S. 300, 1900, Verlag F. Vieweg und Sohn
- ↑ Manfred Georg Krukemeyer, Wolfgang Wagner: Strahlenmedizin: Ein Leitfaden für den Praktiker. Walter de Gruyter, 2004, ISBN 3-11-018090-1, S. 133; eingeschränkte Vorschau in der Google-Buchsuche.
