Wohl-Ziegler-Reaktion
Die Wohl-Ziegler-Reaktion (nach Alfred Wohl und Karl Ziegler) stellt eine radikalische Bromierung von Alkenen in Allylstellung dar. Da die Bromierung eines Alkens zur elektrophilen Addition an der Doppelbindung führt, dürfen nur geringe Mengen Brom vorhanden sein. Dies wird durch eine Komproportionierung mit N-Bromsuccinimid (NBS) erreicht. Die Reaktion läuft nach dem Mechanismus einer radikalischen Substitution ab und wird in unpolaren Lösungsmitteln durchgeführt, zum Beispiel Tetrachlormethan. Das Lösungsmittel bietet den Vorteil, dass das entstehende Succinimid darin nicht löslich ist und somit leicht abgetrennt werden kann. Wird die Reaktion in polaren Solventien durchgeführt, erfolgt eine normale Bromaddition.
Bruttoreaktion am Beispiel des Cyclohexens:
Die Reaktion kann entweder mit Hilfe eines Radikalstarters oder durch UV-Strahlung eingeleitet werden. Als Radikalinitiator können Azobisisobutyronitril (AIBN), Dibenzoylperoxid (DBPO) oder tert-Butylhydroperoxid verwendet werden. NBS enthält in der Regel Spuren von Brom, wodurch die leicht bräunliche Färbung des Salzes zustande kommt. Diese Brommoleküle sind für den Start der Reaktion wichtig, weshalb sie nicht durch Umkristallisation entfernt werden sollten.
Reaktionsmechanismus
Reaktionsmechanismus am Beispiel des Cyclohexens.
Startreaktion:
Als Startreaktion wird durch den Radikalstarter (z. B. AIBN) das molekulare Brom, das in Verunreinigungen im NBS vorhanden sein muss, in zwei Bromradikale gespalten.
Kettenpropagation:
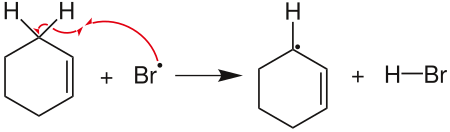
1) H-Abstraktion am Edukt
2) Bildung von Brom und Succinimid durch Komproportionierung des Broms
3) Bildung des Produktes
Literatur
- Reinhard Brückner, Reaktionsmechanismen: Organische Reaktionen, Stereochemie, moderne Synthesemethoden, Spektrum-Lehrbuch, Heidelberg/Berlin 1996 1. Auflage, ISBN 3-86025-363-8