Dichlorsilan
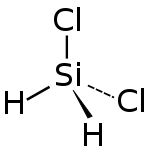
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Dichlorsilan | ||||||||||||
| Andere Namen |
DCS | ||||||||||||
| Summenformel | SiH2Cl2 | ||||||||||||
| Kurzbeschreibung |
hochentzündliches, farbloses Gas mit stechendem Geruch[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 101,01 g·mol−1 | ||||||||||||
| Aggregatzustand |
gasförmig[1] | ||||||||||||
| Dichte | |||||||||||||
| Schmelzpunkt |
−122,0 °C[1] | ||||||||||||
| Siedepunkt |
8,4 °C[1] | ||||||||||||
| Dampfdruck | |||||||||||||
| Löslichkeit |
Hydrolyse in Wasser[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Dichlorsilan ist eine chemische Verbindung aus der Gruppe der chlorierten Silane.
Gewinnung und Darstellung
Dichlorsilan kann durch Chlorierung von Monosilan mit Chlorwasserstoff in Gegenwart von Aluminiumchlorid als Katalysator bei erhöhter Temperatur hergestellt werden.[3]
Daneben kann es durch Disproportionierung von Trichlorsilan an geeigneten Katalysatoren gewonnen werden.[4]
Eigenschaften
Dichlorsilan ist ein hochentzündliches, ätzendes, unter Druck verflüssigtes Gas. Es bildet bei Kontakt mit feuchter Luft einen Chlorwasserstoffnebel. In Wasser hydrolysiert es zu Chlorwasserstoff und einer Mischung von polymeren Siloxanen. Ab einer Temperatur von 55 °C zersetzt sich die Verbindung, wobei Chlorwasserstoff und in geringen Mengen auch Wasserstoff und Chlor entstehen. Es besteht die Gefahr der Selbstentzündung. Der Explosionsbereich liegt zwischen 2,5 Vol.‑% (105 g/m3) als untere Explosionsgrenze (UEG) und 80,0 Vol.‑% (3359 g/m3) als obere Explosionsgrenze (OEG).[5][1] Es ist empfindlich gegenüber Sauerstoff und UV-Licht. Die Verbindung besitzt eine kritische Temperatur von 176,3 °C, einen kritischen Druck von 43,78 bar, eine kritische Dichte von 0,479 kg/l und eine Tripelpunkttemperatur von −122 °C (Schmelztemperatur).[1] Die spezifische Verdampfungsenthalpie beträgt 249 kJ/kg.[6]
Verwendung
Dichlorsilan wird in der Halbleiterproduktion bei der chemischen Gasphasenabscheidung bzw. Epitaxie auch im Gemisch mit Ammoniak bei der Herstellung von Siliciumnitrid oder Siliciumdioxid verwendet.[2]
Sicherheitshinweise
Die Dämpfe von Dichlorsilan können mit Luft ein explosionsfähiges Gemisch (Flammpunkt −28 °C, Zündtemperatur 185 °C) bilden.
Weblinks
- Ansyco: IR-Spektrum von Dichlorsilan
Einzelnachweise
- ↑ a b c d e f g h i j k Eintrag zu Dichlorsilan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ a b Airliquide: Dichlorsilan N30
- ↑
- ↑ Patentanmeldung EP0474265A2: Verfahren zur Herstellung von Dichlorsilan. Angemeldet am 26. März 1988, veröffentlicht am 11. März 1992, Anmelder: Hüls Aktiengesellschaft, Erfinder: Reinhard Matthes et Al.
- ↑ E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- ↑ Datenblatt Dichlorsilan (Memento vom 18. Mai 2015 im Internet Archive) bei Messer Schweiz AG (PDF; 207 kB).




![{\displaystyle \mathrm {SiH_{4}+\ 2\ HCl\ {\xrightarrow[{AlCl_{3}}]{100\,{}^{\circ }C,30h}}\ SiH_{2}Cl_{2}\ +\ 2\ H_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/731182ef6069adf44080f0542e39889f902b5ce1)