Benutzer:Wg0867/Ibogaine
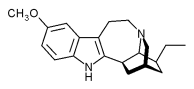 PubChem-Nr.: 363272 | |
| Pharmakologische Kategorie | |
|---|---|
| Rauschdroge | Oneirogen |
| Rechtsstatus | |
| DE / AT | legal |
| CH | nicht legal |
| Geschichte (Chemie) | |
| Isolierung | 1901 Haller&Heckel Dybowski&Landrin |
| Strukturaufklärung | 1958 Taylor |
| Erstsynthese | 1966 Büchi |
| Zentrale Weblinks | |
| |
Ibogain ist ein Indol-Alkaloid mit im weiteren Sinne halluzinogener Wirkung. Es kommt in verschiedenen Hundsgiftgewächsen vor; darunter vor allem Tabernanthe iboga.
Geschichte
Ibogain wurde erstmals 1901 von sowohl von Dybowski und Landrin[1] als auch von Haller und Heckel aus der Wurzelrinde der Tabernanthe iboga isoliert. Im selben Jahr beobachteten französische Pharmakologen eine ungewöhnliche Art der Erregung bei Tieren. Phisalix vermutete eine halluzinogene Wirkung aufgrund des veränderten Verhaltens von Hunden. Nach weiteren klinischen Tests wurde das Alkaloid zur Unterstützung der Rekonvaleszenz und bei Neurasthenie empfohlen, wurde dann aber kaum eingesetzt. In den 1940er Jahren veröffentlichte Raymond-Hamet mit Kollegen Untersuchungen zur pharmakologischen Wirkung auf isoliertes Zellgewebe und das kardiovaskuläre System.
In Frankreich wurde von 1939 bis 1967 ein Stimulans namens Lambarene verkauft. Eine Tablette enthielt 8 mg Ibogain, welches aus Tabernanthe manii, einer Verwandten der Tabernanthe iboga, extrahiert wurde. Ein weiterer Ibogainextrakt, Iperton, wurde als Tonikum verkauft.
Die anspruchsvolle Totalsynthese gelang 1966 G. Büchi.[2] Seitdem wurden weitere totalsynthetische Zugänge entwickelt.[3]
Obwohl Iboga und Ibogain bereits seit 1967 in den USA verboten sind (Schedule I), wurden nur einmal im Jahre 1983 etwa 3 Gramm Ibogain-Hydrochlorid polizeilich beschlagnahmt. Im Dezember 2005 wurde ein Ehepaar wegen geplanter Einfuhr von Ibogain in den USA festgenommen. Dies ist die bisher einzige bekannte Verhaftung wegen Ibogain überhaupt. Der Prozess steht noch aus.[4]
1989 wurde Ibogain in die Dopingliste des Internationalen Olympischen Komitees aufgenommen.
Rechtsstatus
Die Pflanze und deren Inhaltsstoffe sind lt. Bundesopiumstelle (BOPST) in Deutschland bislang nicht dem Betäubungsmittelgesetz unterstellt und daher frei handelbar. Stand: 08/2011. Das Hauptalkaloid in Tabernanthe iboga ist Ibogain.
Die Alkaloide in T. iboga lassen sich in drei Gruppen einteilen. Iboga-Typ: Ibogain (12-Methoxy-Ibogamin), Tabernanthin, Ibogamin, Ibogalin, Gabonin, dem Voacangin-Typ: Voacangin, Catharanthin, Voacyptin, Coronaridin und dem Voaphyllin-Typ: Voaphyllin
Wirkung
Ibogain wirkt in geringen Dosen stimulierend. Höhere Dosierungen (ab 5-10 mg/kg Körpergewicht) lösen Visionen aus, d.h. bei geschlossenen Augen werden in einer Art traumähnlichem Erleben schnelle Abfolgen von Bildern und Filmen gesehen, oft mit intensivem emotionalem und auch religiös-mystischem Empfinden. Halluzinationen bei geöffneten Augen treten hingegen kaum auf. Daher ist die Wirkung nicht mit der von bekannteren Psychedelika wie LSD vergleichbar. Es wurde vorgeschlagen statt halluzinogen das Wort oneirisch, d.h. Traum-erzeugend, zu verwenden.
Die Wirkung hält zwischen acht und zwölf Stunden an wobei die akut visionäre Phase nur vier bis acht Stunden dauert. Rund ein Fünftel der Konsumenten berichtet von subjektiven Nachwirkungen noch 24 Stunden nach der Einnahme, 15 Prozent sogar noch nach 36 Stunden.
Noch höhere Dosierungen führen zu Krämpfen, Lähmungserscheinungen und können im Tod durch Atemstillstand enden. Des weiteren besteht die Gefahr von Herzrhythmusstörungen, was im schlimmsten Fall zum plötzlichem Herztod führen kann.
Es vermindert den Blutdruck, den Appetit und die Verdauungstätigkeit und ist daher möglicherweise auch ein Cholinesterasehemmer.
Verwendung
Drogenentzug
In den 1960er Jahren entdeckte Howard Lotsof die suchtunterbrechende Wirkung von Ibogain und erhielt in den 1980er und 90er Jahren mehrere US-Patente für die Therapie mit Ibogain.
Seit Mitte der 1980er Jahre bieten Selbsthilfeorganisationen und Privatleute, aber auch Ärzte, den Entzug mit Ibogain an, sowohl in klinischer wie auch in informeller Umgebung. Während Ibogain in den meisten Ländern zwar nicht als Medikament zugelassen, aber auch nicht illegal ist, hat sich in den USA aufgrund des dortigen Verbots eine Untergrundbewegung gebildet.
Der genaue Wirkungsmechanismus, nach dem das Alkaloid Abhängigkeiten durchbrechen soll, ist nicht bekannt. Probanden, denen Ibogain verabreicht wurde, beschrieben wiederholt, dass sie während des Rausches Situationen wiedererlebt hatten, die ihrer Meinung nach für ihre Abhängigkeit ausschlaggebend waren. Andere berichteten von Visionen, die ihnen halfen, die ihrer Sucht zugrundeliegenden Ängste zu erkennen und zu überwinden.
Pharmakologie
Die Pharmakologie des Ibogains ist relativ komplex, es bindet schwach bis moderat an eine ganze Reihe unterschiedlichster Rezeptoren.[5] [6] Wegen dieser geringen Selektiviät im Wirkprofil wird diese Droge als "schmutzig" bezeichnet. Da offenbar zu keinem Rezeptor eine besonders hohe Affiniät besteht, ist die übliche Anwendungsdosis im Bereich von zehntel Gramm bis zu einem Gramm recht hoch.
Bindungsprofil
Ibogain blockiert den NMDA-Kanal spannungsabhängig, in einer dem Memantin vergleichbaren Weise. Es bindet an den Serotonin-Transporter und um einiges schwächer auch an den Dopamin-Transporter, nicht aber am Noradrenalin-Transporter. Ibogain bindet an vesikuläre Monoamintransporter via Tetrabenazin-Bindungsstelle, eine Korrelation ist denkbar zur dem Fenfluramin ähnlichen Serotonin-Release-Wirkung[7] und zum gesteigerten Dopamin-Abbau. Ibogain wirkt als schwacher kappa-Opioidrezeptor-Agonist, schwacher 5-HT2A-Antagonist und schwacher 5-HT3-Ligand. Moderate Affinität hat Ibogain zu Sigma2-Bindungsstellen, an denen es agonistisch wirkt. Affinität hat es an Nikotin-Rezeptoren, dabei moderat am Subtyp alpha4beta2 und ausgeprägter (fünfmal stärker) an alpha3beta4, hier wirkt es als Kanalblocker, d.h. als nicht-kompetiver Antagonist.
Der Hauptmetabolit O-Noribogain ist etwas stärker kappa-agonistisch als Ibogain und wirkt zudem als schwacher mü-Agonist. Insbesondere hemmt Noribogain die Serotonin-Wiederaufnahme (vergl. SSRI).
Chemie
| Chemisch-physikalische Daten | |
|---|---|
| Summenformel | C20H26N2O |
| Molmasse | 310,44 g/mol |
| Aggregatzustand | fest |
| Schmelzpunkt | 153 °C (Base) |
| Säurekonstante | 8,1 |
| Drehwinkel | -53° (EtOH) (Base) -63° (EtOH) (HCl) -49° (H2O) (HCl) |
| Toxizität | |
| LD50 Meerschwein | 82 mg/kg (i.p.) |
| LD50 Ratte | 145 mg/kg (i.p.) |
| LD50 Ratte | 327 mg/kg (intragastrisch) |
| Analysespektren | |
| . | |
| Literatur | |
| CAS-Nummer | 83-74-9 |
| Beilstein | |
| Merck | |
Baustelle
| Andere Namen || 12-Methoxy-Ibogamin | Löslichkeit || als Hydrochlorid mäßig in Wasser, als freie Base gut in unpolaren Lösungsmitteln
|- style="background:#ffdead;" ! colspan="2" | Gefahrensymbole |- | colspan="2" align="center" |

|
T Giftig |
Referenzen
- ↑ J. Dybowski, E. Landrin C. R. Acad. Sci. 1901, Vol. 133, S. 748. (pdf, engl.)
- ↑ G. Büchi J. Am. Chem. Soc. 1966, Vol. 88 (13), S. 3099-3109 (pdf, engl.)
- ↑ C. Frauenfelder Dissertation 1999, S. 24 (pdf)
- ↑ Zeitungsmeldung: Star-Tribune vom 09.12.2005. (engl.)
- ↑ P. Popik, P. Skolnick (1998). Pharmacology of Ibogaine and Ibogaine-Related Alkaloids. The Alkaloids 52, Kapitel 3, 197-231, Academic Press, Editor: G.A. Cordell (engl.)
- ↑ K.R. Alper (2001). Ibogaine: A Review. The Alkaloids 56, 1-38, Academic Press (pdf, engl.)
- ↑ D. Wei: Acute iboga alkaloid effects on extracellular serotonin levels in nucleus accumbens and striatum in rats. In: Brain Res.. 800(2), 1998, S. 260. PMID 9685673.