Dithiane
Dithiane sind heterocyclische Verbindungen die aus einer Cyclohexanstruktur bestehen, in der zwei Methylengruppen durch Schwefelatome ersetzt sind. Es existieren drei isomere Formen, das 1,2-Dithian, das 1,3-Dithian und das 1,4-Dithian.
1,2-Dithiane
1,2-Dithiane bilden aufgrund der möglichen Diederwinkel der Schwefel-Schwefel-Bindung verschiedene Enantiomere.[1]
1,3-Dithiane
1,3-Dithiane sind aufgrund ihres inerten Verhaltens gegen verschiedene Synthesebedingungen eine gute Schutzgruppe für Carbonylgruppen. Sie bilden sich bei der Umsetzung der Carbonylverbindung mit 1,3-Propanthiol unter Bildung von Wasser. Die Schutzgruppe kann mit Quecksilberverbindungen wie Quecksilber(II)-chlorid der Quecksilber(II)-oxid entfernt werden. Aufgrund des sehr unangenehmen Geruchs von 1,3-Propanthiol sind auch alternative Reagenzien für die Bildung der 1,3-Dithiane entwickelt worden.[2] 1,3-Dithiane wurden in der Totalsynthese von Naturstoffen eingesetzt.[3]
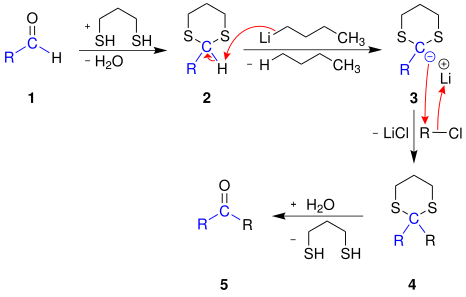
1,3-Dithiane werden beispielsweise in der Corey-Seebach-Reaktion als Schutzgruppe für die Umpolung von Carbonylverbindungen mit lithiumorganischen Verbindungen wie Butyllithium eingesetzt.[4]
1,4-Dithiane
1,4-Dithiane können durch Reduktion von 1,2-Ethandithiol mit metallischen Natrium und anschließender Umsetzung unter geeigneten Bedingungen mit 1,2-Dibromethan erhalten werden.[5] Als Hauptprodukte bilden sich jedoch polymere Strukturen. Die thermische Zersetzung dieser Polymere führt ebenfalls zur Bildung von 1,4-Dithian.
Weblinks
Einzelnachweise
- ↑ Göran Claeson, Gaylord M. Androes, Melvin Calvin: The Energy Barrier between the Enantiomers of 1,2-Dithiane . In: Journal of the American Chemical Society. 82, 1960, S. 4428–4429, doi:10.1021/ja01501a077.
- ↑ Qun Liu, Guangbo Che, Haifeng Yu, Yingchun Liu, Jingping Zhang, Qian Zhang, Dewen Dong: The First Nonthiolic, Odorless 1,3-Propanedithiol Equivalent and Its Application in Thioacetalization. In: The Journal of Organic Chemistry. 68, 2003, S. 9148–9150, doi:10.1021/jo034702t.
- ↑ Miguel Yus, Carmen Najera, Francisco Foubelo: The role of 1,3-dithianes in natural product synthesis. In: Tetrahedron. 59, 2003, S. 6147–6212, doi:10.1016/S0040-4020(03)00955-4.
- ↑ Bengt-Thomas Gröbel, Dieter Seebach: Umpolung of the reactivity of carbonyl compounds through sulfur-containing reagents. In: Synthesis, 1977.6 (1977): S. 357–402.
- ↑ N. Beverley Tucker, E. Emmet Reid: Cyclic and Polymeric Compounds from the Reactions of Ethylene Mercaptan with Polymethylene Halides. In: Journal of the American Chemical Society. 55, 1933, S. 775–781, doi:10.1021/ja01329a052.