Gallium(I,III)-iodid
aus Wikipedia, der freien Enzyklopädie
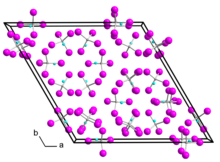
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Ga+ _ Ga3+ _ I− | ||||||||||
| Allgemeines | ||||||||||
| Name | Gallium(I,III)-iodid | |||||||||
| Andere Namen |
| |||||||||
| Verhältnisformel | GaI2 | |||||||||
| Kurzbeschreibung |
gelber Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 323,5 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gallium(I,III)-iodid ist eine anorganische chemische Verbindung des Galliums aus der Gruppe der Iodide.
Gewinnung und Darstellung
Gallium(I,III)-iodid kann durch Reaktion von Gallium mit Iod bei 350 °C oder mit Quecksilber(II)-iodid bei 220 °C gewonnen werden.[1]
Eigenschaften
Gallium(I,III)-iodid ist ein gelber hygroskopischer diamagnetischer Feststoff.[1] In flüssiger Form ist er rot.[3] Er disproportioniert bei 250 °C leicht zu Gallium(I)-iodid und Gallium(III)-iodid.[1] Die Verbindung liegt in fester Form als Ga[GaI4] vor.[4]
Einzelnachweise
- ↑ a b c d e f Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 855.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Jane E. Macintyre: Dictionary of Inorganic Compounds. CRC Press, 1992, ISBN 0-412-30120-2, S. 3304 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Egon Wiberg, Nils Wiberg: Inorganic Chemistry. Academic Press, 2001, ISBN 0-12-352651-5, S. 1036 (eingeschränkte Vorschau in der Google-Buchsuche).

