Hautflora
Als Hautflora werden alle Mikroorganismen, wie Bakterien und Pilze, zusammengefasst, die als Kommensalen bzw. Mutualen einen natürlichen Bestandteil der Oberfläche von gesunder Haut bilden und diese dicht besiedeln. Die Hautflora ist Teil des Mikrobioms und trägt wesentlich dazu bei, die Haut und den gesamten Organismus vor Krankheitserregern zu schützen.
Die Bezeichnung Hautflora stammt aus einer Zeit, als man Bakterien und Pilze noch als Pflanzen ansah und folgerichtig als Bestandteil der Flora. Heute ist die Bezeichnung Hautmikrobiom treffender (siehe Mikrobiom).
Sofern die Haut als Grenzorgan zur Außenwelt intakt ist und damit ihrer Barrierefunktion nachkommen kann, stören diese Mikroorganismen nicht, machen nicht krank und sind aus mehreren Gründen nützlich. So konkurrieren die Kommensalen z. B. mit fremden Mikroorganismen um ihr „Revier“: Bevor sich der fremde Mikroorganismus auf der Haut ansiedeln kann, muss zunächst der dort ansässige (residente) Platzhalter verdrängt worden sein. Nur Erreger, die sich gegen die Standortflora durchsetzen, können sich vermehren. Zudem erzeugen die residenten Mikroorganismen der Hautflora Stoffwechselprodukte, die sich günstig auf die Funktionen der Haut auswirken.
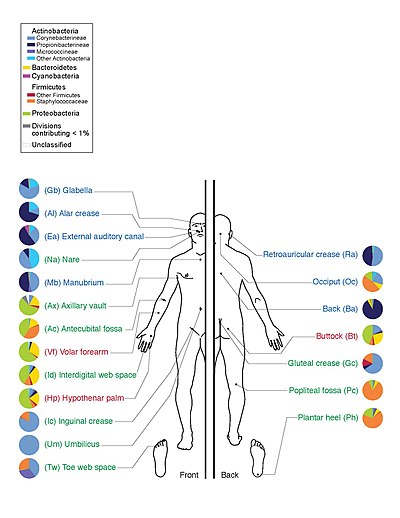
Die einzelnen Hautregionen weisen eine recht unterschiedliche Zusammensetzung an Mikroorganismen auf. Die Haarfollikel beherbergen den Großteil der Mikroorganismen, was u. a. entscheidend für die Ausbildung von Hautkrankheiten wie Akne oder Follikulitis ist.
Bestandteile der Hautflora
Je nach Hautregion, Alter, Geschlecht, genetischer Veranlagung und Umgebungsbedingungen können sowohl das Keimspektrum als auch die Anzahl der Mikroorganismen der Hautflora sehr unterschiedlich sein. So fand eine Studie der New York University, welche die Mikroben auf den Unterarmen von sechs Personen untersuchte, insgesamt 182 verschiedene Bakterien-Arten aus acht Stämmen, wobei jedoch nur vier Arten auf allen sechs Personen nachweisbar waren.[1] Das Verhältnis von anaeroben zu aeroben Arten ist mit 10:1 vergleichsweise ausgeglichen. Die Keimdichten liegen, je nach Region, zwischen 102 und 106 pro cm². Ungefähre Keimzahlen unterschiedlicher Hautregionen (Keimzahl pro cm²): Fingerkuppen 20 – 100, Rücken 3 × 102, Füße 102 – 103, Vorderarm 102 – 5 × 103, Hand 103, Stirn 2 × 105, Kopfhaut 106, Achselhöhle 2 × 106. Insgesamt leben rund 1010 Bakterien auf unserer Hautoberfläche.
Dabei wird unterteilt in residente und transiente Hautflora.
Residente Flora
Die residente Flora oder auch Standortflora ist Teil der physiologischen Beschaffenheit der Haut. Die zugehörigen Mikroorganismen befinden sich im Stratum corneum der Hornschicht und den Ausführungsgängen von Talgdrüsen bzw. Haarfollikeln.[2] Sie erschweren als Platzhalter die Ansiedlung nichtresidenter Keime und sorgen auf diese Weise für die sogenannte Kolonisationsresistenz.[3] Durch ihre Stoffwechselprodukte halten sie die normalen Hautfunktionen aufrecht und hemmen zusätzlich das Wachstum nichtresidenter Keime. Gelangen residente Mikroorganismen jedoch ins Körperinnere – z. B. bei nicht intakter Haut oder durch invasive Eingriffe – können auch sie Infektionen verursachen.
Staphylokokken (S. epidermidis, S. saprophyticus, S. hominis, S. xylosus, S. warneri, S. haemolyticus, S. saccharolyticus, S. conii, S. auricularis) besiedeln bevorzugt feuchte und talgarme Hautregionen, wie intertriginöse Bereiche, Hände und Füße.
Corynebakterien (C. minutissimum, C. jeikeium, C. xerosis, C. pseudotuberculosis, C. goutcheri, C. pseudodiphteriticum, C. bovis) spalten die von den Talgdrüsen der Haut gebildeten Fette zu Fettsäuren, die für das saure Milieu auf der Haut mitverantwortlich sind und damit ihrerseits wieder zu einer Hemmung des Keimwachstums führen.
Brevibacterium und Dermabacter verursachen u. a. den individuellen Körpergeruch.
Mikrokokken (M. luteus, M. flavus) sind besonders bei Kindern nachweisbar.
Weitere Bakterien sind apathogene Mykobakterien, Sarcinia spp., Propionibakterien (P. acnes, P. granulosum, P. avidum), Enterokokken und Acinetobacteria.
Während die Haut der Füße eine diverse Pilzflora aufweist, leben auf allen anderen Hautpartien vorwiegend Arten der Gattung Malassezia.[4] Produzieren die Talgdrüsen eines Menschen zu viel Talg oder sind diese Talgdrüsen durch Talg verstopft, dann wird dem normalerweise harmlosen Hefepilz Pitysporum ovale ein verstärktes Wachstum ermöglicht, was zum Seborrhoischen Ekzem mit Juckreiz und Schuppenbildung führt. Schuppen lassen sich mit geeigneten Shampoos inzwischen gut in den Griff bekommen.
Besiedelung der Haarfollikel
Hier finden sich besonders hohe Keimzahlen überwiegend lipophiler Bakterienarten. 20 % der gesamten Hautflora ist in tiefen Abschnitten der Haarfollikel angesiedelt. Nahe der Oberfläche siedeln Staphylokokken und Malassezia, darunter aerobe Corynebakterien und in der Tiefe anaerobe, lipophile Bakterien (Propionibakterium). Diese Mikroorganismen sind auch durch eine Hautdesinfektion nicht zu eliminieren, sie bilden das Reservoir, aus dem sich die Hautflora nach der Desinfektion innerhalb von 24 bis 72 Stunden erneut bildet.
Haarbalgmilbe
Haarbalgmilben wie Demodex folliculorum leben in den Haarfollikeln der Haut. Haarbalgmilben werden von Person zu Person weitergegeben, meist von Mutter zu Kind, und besiedeln jeden Menschen, aber auch Hunde und Katzen. Die winzigen Milben fressen Fett, Bakterien, aber auch Cremereste und Schminke. Nach zwei Wochen Leben auf der Haut kehren sie an ihren Geburtsort, das Haarfollikel, zurück, wo sie sich paaren und Eier ablegen. Die neuen Milben wandern mit dem wachsenden Haar wieder auf die Hautoberfläche zurück. Ihre Existenz hilft, das Gleichgewicht auf der Haut aufrechtzuerhalten. Während sie bei Tieren mit geschwächtem Immunsystem Räude verursachen können, sind negative Folgen bei Menschen und seinem Partner Demodex folliculorum nicht bekannt.
Transiente Keimbesiedelung
Die transiente Hautflora besteht aus Mikroorganismen, die bestimmte Hautregionen vorübergehend besiedeln. Darunter befinden sich möglicherweise auch krankheitsverursachende (pathogene) Erreger. Sie können aus der Umgebung oder vom eigenen Körper – z. B. Nasensekret, Darmbakterien – stammen.[5]
Staphylococcus aureus, E. coli, Klebsiella, Pseudomonas und Enterobacteriaceaen kommen an feuchten und warmen Hautregionen (intertriginöse Bereiche) häufiger vor. Weitere Mikroorganismen der transienten Keimbesiedelung sind aerobe grampositive Sporenbildner.
Eine hygienische Händedesinfektion kann die transiente Hautflora der Hände so stark reduzieren, dass eine Verbreitung bzw. Übertragung von Krankheitserregern weitgehend verhindert wird.[6]
Einflussfaktoren
Feuchtigkeit, pH-Wert und Sauerstoffversorgung sind je nach Hautbereich sehr unterschiedlich, dementsprechend ist auch die Verteilung der Bakterien der Hautflora nicht gleichmäßig.
Hornschicht
Abgesehen von denjenigen Mikroorganismen, die sich auf den Abbau des Keratins spezialisiert haben (Dermatophyten, Trichophyten), ist das Nährstoffangebot der Hautoberfläche eingeschränkt und somit bei weitem nicht für alle Bakterien ideal. Einer Invasion steht zudem das stetige Wachstum der Epidermis entgegen, denn die am stärksten besiedelten Zellschichten (Stratum disjunctum des Stratum corneum) werden kontinuierlich abgestoßen.
Hautoberflächen-pH-Wert
Es ist seit langem bekannt, dass die Hautoberfläche sauer reagiert (Heuss 1882), später sprach man auch vom „Säureschutzmantel der Haut“ (Schade/Marchionini 1928). Es wurden zahlreiche Untersuchungen zum Hautoberflächen-pH-Wert gemacht und lange galt der viel zitierte pH-Bereich von 5,4–5,9 als der Normalwert am „Unterarm eines weißen, männlichen, erwachsenen Individuums“ (Braun-Falco/ Korting 1986). Zwei aktuelle Studien haben gezeigt, dass der physiologische pH-Wert knapp unter 5 liegt (Lambers et al. 2006; Segger et al. 2007). Darüber hinaus wird der pH-Wert von zahlreichen Faktoren beeinflusst, wie z. B. Alter, Geschlecht, Hautareal, Kosmetika etc.
Die Bedeutung des leicht sauren pH-Werts wurde ebenfalls in zahlreichen Studien untersucht und es konnte gezeigt werden, dass durch ihn das Wachstum von einigen pathogenen Mikroorganismen (z. B. Propionibacterium acnes) gehemmt wird, aber die Mikroorganismen der Normalflora (z. B. Staphylococcus epidermidis) sehr gut bei einem pH-Wert um 5 wachsen. Somit wird durch den „Säureschutzmantel“ das Wachstum von nicht-pathogenen Bakterien stabilisiert und das von pathogenen gehemmt (Pillsbury/Rebell 1952; Korting et al. 1987, 1990 und 1992; Kurabayashi et al. 2002; Lambers et al. 2006).
Darüber hinaus funktionieren durch den pH-Wert der Hautoberfläche viele pH-abhängige Enzyme sehr gut, die an dem Aufbau und der Regeneration der epidermalen Permeabilitätsbarriere (Hautbarriere) beteiligt sind. Somit ist der leicht saure Haut-pH-Wert von entscheidender Bedeutung für die gesamte Homöostase der Haut.
Trockenheit
Trotz der Schweißdrüsen und transdermaler Flüssigkeitsabsonderung (Perspiratio insensibilis) bietet die Epidermis ein sehr trockenes Milieu, das einen schlechten Nährboden darstellt. Dem entsprechen die deutlich höheren Keimdichten in feuchten Hautbereichen (Intertrigines) wie Achselhöhlen, Finger- und Zehenzwischenräumen, Leistenbeuge und Analfalte.
Lipide, Fettsäuren
Freie Fettsäuren, die teilweise erst durch bakteriellen Metabolismus gebildet werden (lipophile Mikroorganismen, siehe unten), wirken auf viele Bakterienarten bakterizid. Eine Veränderung dieser Milieubedingungen zieht auch Verschiebungen in den Keimdichten der einzelnen Arten und Spezies nach sich. So nimmt beispielsweise der Anteil lipophiler Arten im Zustand der Seborrhoeae zu und die allgemeine Keimzahl steigt bei vermehrter Schweißbildung (Befeuchtung ansonsten trockener Haut) an.
Hautregionen mit besonderen Milieueigenschaften
Seborrhoische Zonen
Talgreiche Hautregionen sind besonders dicht mit lipophilen Mikroorganismen besiedelt, hierzu gehören: Corynebakterien, Propionibakterien und Malassezia furfur. Der lipolytische Stoffwechsel der Propionibakterien (u. a. durch Lecithinasen) führt zur Bildung freier Fettsäuren, die wiederum Einfluss nehmen auf die übrige Besiedelung der Haut. Neben diesen lipophilen Mikroorganismen (überwiegend Propionibakterien) sind auch reichlich koagulasenegative Staphylokokken und apathogene Mykobakterien vorhanden. Zu den seborrhoischen Zonen gehören: Stirn, Nasolabialfalte, Nase, Nacken und Schultern.
Feuchte Hautbereiche
Erhöhte Feuchtigkeit führt zu einer Zunahme der Keimdichte. In den intertriginösen Bereichen (Finger- und Zehenzwischenräume, Leistenbeuge, Achselhöhle, Analfalte) sind die Keimzahlen deutlich größer als z. B. an den recht trockenen Unterschenkeln. Die Achselhöhlen sind sehr unterschiedlich besiedelt, entweder überwiegen koagulasenegative Staphylokokken neben wenigen Corynebakterien oder umgekehrt. In den Schweißdrüsengängen siedeln sich Peptostreptokokken an, die nicht selten zur Ursache eines Schweißdrüsenabszesses werden.
Zehenzwischenräume: Pigmentbildende Bacteroides-Spezies (B. melaninogenicus, B. asaccharolyticus) und Clostridium perfringens sind regelmäßig nachweisbar. Intertriginöse Bereiche sind relativ häufig mit (Hefe-)Pilzen besiedelt.
Trockene Hautbereiche
Zum Beispiel die Beugeseite der Unterarme: Insgesamt geringe Keimzahl. Koagulasenegative Staphylokokken überwiegen (102 – 103 KBE/cm²). Nur wenige Corynebakterien und Propionibakterien.
Bestimmung der Keimzahl auf der Haut (Detergenswaschmethode)
Ein Hautbereich definierter Größe wird mit einem bestimmten Volumen Detergens-Lösung überschichtet. Die Mikroorganismen der Hautoberfläche werden durch starkes Reiben im Detergens gelöst und nach einer Verdünnung angezüchtet.
Quellen
- Jörg Blech: Leben auf dem Menschen. Rowohlt, Reinbek 2000; überarbeitete Neuausgabe ebd. 2010, ISBN 978-3-499-62494-0
- Peter Brooke: Kleine Ungeheuer, Die geheime Welt der winzigen Lebewesen, Gondrom-Verlag, 1999, S. 32/33
Weblinks
Einzelnachweise
- ↑ Robert L. Dorit: Körpermikroben - Bevor wir uns zu Tode siegen. In: Spektrum der Wissenschaft. September 2008, S. 62–66
- ↑ A. Kramer, D. Gröschel, P. Heeg, V. Hingst, Hans Lippert, M. Rotter, W. Weuffen (Hrsg.): Klinische Antiseptik. Springer Verlag, Berlin 1993, S. 107; ISBN 978-3-642-77716-5.
- ↑ Christian Jassoy, Andreas Schwarzkopf: Hygiene, Infektologie, Mikrobiologie. 3. Auflage, Georg Thieme Verlag, Stuttgart 2018, S. 40; ISBN 978-3-13-241368-9.
- ↑ Keisha Findley, Julia Oh u. a.: Topographic diversity of fungal and bacterial communities in human skin. In: Nature. 2013, S. , doi:10.1038/nature12171.
- ↑ Christian Jassoy, Andreas Schwarzkopf: Hygiene, Infektologie, Mikrobiologie. 3. Auflage, Georg Thieme Verlag, Stuttgart 2018, S. 195; ISBN 978-3-13-241368-9.
- ↑ Axel Kramer: Händehygiene – Patienten- und Personalschutz. Übersichtsarbeit, GMS Krankenhaushyg Interdiszip 2006;1(1):Doc14; abgerufen am 20. Dezember 2019