Mangan(II)-carbonat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
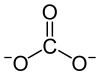
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Mangan(II)-carbonat | |||||||||||||||
| Andere Namen |
Mangancarbonat (mehrdeutig) | |||||||||||||||
| Summenformel | MnCO3 | |||||||||||||||
| Kurzbeschreibung |
farbloser bis hellbrauner geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 114,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
3,12 g·cm−3 (Monohydrat)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−894,1 kJ/mol[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Mangan(II)-carbonat ist eine chemische Verbindung aus der Gruppe der Manganverbindungen und Carbonate.
Vorkommen
Natürlich kommt Mangan(II)-carbonat als Mineral Rhodochrosit vor.
Gewinnung und Darstellung
Mangan(II)-carbonat kann durch Reaktion von gelösten Mangan(II)-Salzen mit alkalischen Carbonaten (z. B. Reaktion von Mangansulfat mit Ammoniumcarbonat gewonnen werden).[4]
Eigenschaften
Mangan(II)-carbonat ist ein in reinem Zustand farbloser, leicht oxidiert bereits ein hellbrauner (als Mineral rosa bis roter) geruchloser Feststoff. Ab einer Temperatur von 200 °C zersetzt es sich, wobei Manganoxide und Kohlendioxid frei werden.
Verwendung
Mangan(II)-carbonat wird als Düngemittelzusatz, Zusatz zur Verbesserung der dielektrischen Eigenschaften von Bariumtitanat und zur Herstellung von Ferriten und anderen Manganverbindungen verwendet.[1] Das Monohydrat wird auch zur Färbung (lila bis violett[5]) von Keramik eingesetzt.[6]
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Mangan(II)-carbonat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 22. Dezember 2019. (JavaScript erforderlich)
- ↑ a b National Pollutant Inventory: Manganese & compounds, abgerufen am 17. Februar 2015.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-20.
- ↑ Martha Austin: Über die Bestimmung von Mangan als Karbonat. In: Zeitschrift für anorganische Chemie. 1898, 17 (1), S. 272–275; doi:10.1002/zaac.18980170127.
- ↑ Seite nicht mehr abrufbar, Suche in Webarchiven: Keramische Rohstoffe (ceramicashop) (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis. (PDF; 110 kB)
- ↑ Mangancarbonat (Todini and Co.) (Memento des Originals vom 15. Mai 2016 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
