Myers-Saito-Cyclisierung
Die Myers-Saito-Cyclisierung, Myers-Saito-Reaktion oder auch Myers-Umlagerung genannt, ist eine Namensreaktion der organischen Chemie, welche auf die Chemiker Andrew G. Myers und Isao Saito zurückgeht. Die Reaktion wurde erstmals 1989 als eine intermolekulare Umlagerung von Eninallene veröffentlicht.[1][2]
Übersichtsreaktion
Bei der Myers-Saito-Cyclisierung wird z. B. cis-1,2,4-Heptatrien-6-in (1) zu Toluol (2) umgelagert.[1]
Dieses Reaktionsprinzip ist auf Derivate von cis-1,2,4-Heptatrien-6-in übertragbar.
Reaktionsmechanismus
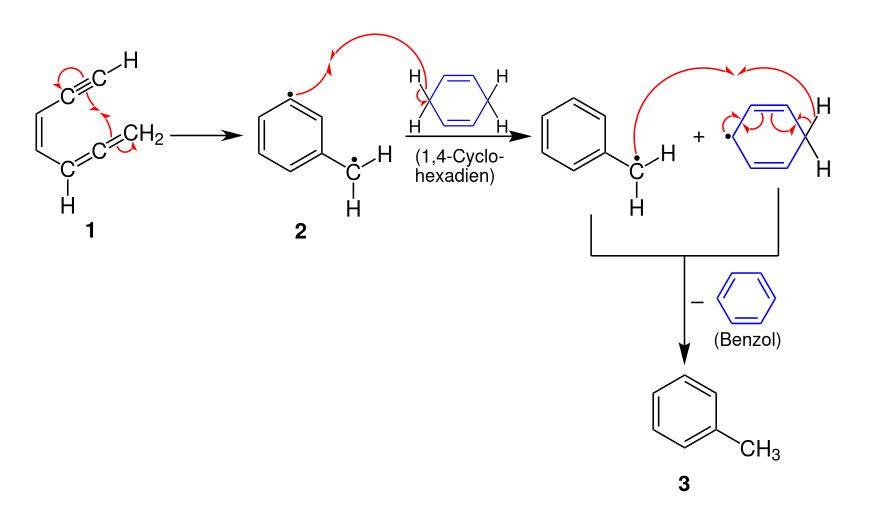
Ein möglicher Reaktionsmechanismus für die Myers-Saito-Cyclisierung wird von Zerong Wang wie folgt beschrieben:[1]
Das cis-1,2,4-Heptatrien-6-in (1) bildet durch eine intermolekulare Umlagerung das 1-Phenylmethyldiradical (2). Das 1,4-Cyclohexadien dient als Protonen-Lieferant und protoniert das Diradikal zum Produkt Toluol (3).[1]
Anwendung
Die Myers-Saito-Cyclisierung findet Anwendung in der präparativen Chemie zur Synthese von polycyclischen aromatischen Ringsystemen.[1]
Siehe auch
Bergman-Cyclisierung und Schmittel-Cyclisierung
Einzelnachweise
- ↑ a b c d e Zerong Wang: Comprehensive Organic Name Reactions and Reagents, Volume 2. John Wiley, Hoboken (N.J.) 2009, ISBN 978-0-470-28662-3, S. 2003–2006.
- ↑ B. P. Mundy, M. G. Ellerd und F. G. Favaloro Jr. (Hrsg.): Name Reactions and Reagents in Organic Synthesis, Secound Edition. John Wiley & Sons, Hoboken, NJ 2005, ISBN 0-471-22854-0, S. 444.