Niobcarbid
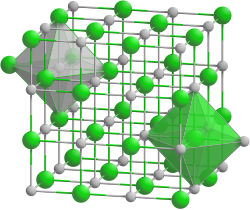
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Nb4+ _ C4− | ||||||||||
| Allgemeines | ||||||||||
| Name | Niobcarbid | |||||||||
| Verhältnisformel | NbC | |||||||||
| Kurzbeschreibung |
grauer geruchloser Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 104,91 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Dichte |
7,60 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
4300 °C[2] | |||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| MAK |
Schweiz: 5 mg·m−3 (gemessen als einatembarer Staub)[3] | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Niobcarbid ist eine intermetallische Verbindung aus Niob und Kohlenstoff mit der Summenformel NbC aus der Gruppe der Carbide. In der Natur ist Niobcarbid sehr selten als Mineral Niobocarbid zu finden.[4][5]
Darstellung
Niobcarbid wird durch Umsetzung von Niob- mit Kohlenstoffpulver im Vakuum oder einer Wasserstoffschutzatmosphäre dargestellt.[6]
Kleine Mengen der Niobcarbid können aus Niobdrähten bei Temperaturen über 2500 °C in einer Wasserstoffatmosphäre mit Zusatz geringer Mengen von Kohlenwasserstoffen (z. B. Toluol, Methan, Acetylen) erhalten werden. Ebenfalls möglich ist die Herstellung durch Reaktion von Nioboxiden und Kohlenstoff.[6]
Eigenschaften und Verwendung
Niobcarbid ist ein eisengraues bis dunkelgraues Pulver, das im kompakten, gesinterten Zustand mehr oder weniger metallisch glänzt. Durch Anlauffarben ist es manchmal oberflächlich braun bis gelblich gefärbt.[6] Es hat einen Homogenitätsbereich von NbC0,7 bis NbC0,99 und oxidiert ab 800 °C.[7] Es hat eine kubische Kristallstruktur vom Natriumchloridtyp mit der Raumgruppe Fm3m (Raumgruppen-Nr. 225).[8] Es hat eine Mohshärte von 9+, ist damit ein Hartstoff und ist löslich in einer Mischung von Flusssäure und Salpetersäure.[9] Mit Nb2C ist ein weiteres Niobcarbid (CAS-Nummer 12011-99-3) mit hexagonaler Kristallstruktur und einer Schmelztemperatur von 3080 °C bekannt.[2]
Verwendung
Niobcarbid wird als Zusatz zu Spezialstählen (es erhöht die Verschleißfestigkeit, wodurch diese Stähle zum Beispiel für Kolbenringe eingesetzt werden[10]), zur Beschichtung von Graphit für Kernreaktoren und als Sputtermaterial zur Herstellung von Halbleiterfilmen verwendet.[9]
Aus Niobcarbid und Niob(V)-oxid wird bei 2000 °C reines Niob gewonnen.[11]
Einzelnachweise
- ↑ a b c d e f g Datenblatt Niobium carbide, 99+% (metals basis) bei AlfaAesar, abgerufen am 27. Juni 2013 (PDF) (JavaScript erforderlich).
- ↑ a b W. M. Haynes, David R. Lide, Thomas J. Bruno: CRC Handbook of Chemistry and Physics 2012–2013. CRC Press, 2012, ISBN 1-4398-8049-2, S. 4–78 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 12069-94-2 bzw. Niobcarbid), abgerufen am 2. November 2015.
- ↑ Mineralienatlas:Niobocarbid
- ↑ Niobocarbide. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (handbookofmineralogy.org [PDF; 62 kB; abgerufen am 24. Februar 2018]).
- ↑ a b c Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1475.
- ↑ Hugh O. Pierson: Handbook of Chemical Vapor Deposition, 2nd Edition: Principles, Technology ... William Andrew, 1999, ISBN 0-08-094668-2, S. 241 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Roger Blachnik (Hrsg.): Taschenbuch für Chemiker und Physiker. Band III: Elemente, anorganische Verbindungen und Materialien, Minerale. begründet von Jean d’Ans, Ellen Lax. 4., neubearbeitete und revidierte Auflage. Springer, Berlin 1998, ISBN 3-540-60035-3, S. 632 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis, 2011, ISBN 1-4398-1462-7, S. 488 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ernst Brunhuber, Stephan Hasse: Giesserei-Lexikon. Fachverlag Schiele & Schoen, 2001, ISBN 3-7949-0655-1, S. 909 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Karl-Heinz Lautenschläger: Taschenbuch der Chemie. Harri Deutsch Verlag, 2007, ISBN 978-3-8171-1761-1, S. 554 (eingeschränkte Vorschau in der Google-Buchsuche).


