Propionitril
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
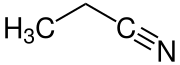
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Propionitril | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C3H5N | ||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit etherischem Geruch[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 55,08 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Dichte | |||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt |
97 °C[1] | ||||||||||||
| Dampfdruck | |||||||||||||
| Löslichkeit |
| ||||||||||||
| Brechungsindex |
1,3655 (20 °C)[3] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||
| ΔHf0 |
15,5 kJ/mol[6] | ||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||
Propionitril (systematischer Name Propannitril) ist eine chemische Verbindung aus der Gruppe der Nitrile. Der Trivialname leitet sich von der Propionsäure ab.
Gewinnung und Darstellung
Die erste Synthese von Propionitril (und damit des ersten Nitrils überhaupt) wurde 1834 von Théophile-Jules Pelouze beschrieben, der die Verbindung durch Reaktion von Kaliumcyanid mit Kaliumethylsulfat gewann. Die Reaktion von Dialkylsulfaten mit Alkalimetallcyaniden ist dabei eine allgemeine Synthesemethode für aliphatische Nitrile. In allen Fällen ist das einzige Alkylierungsprodukt das entsprechende Alkylcyanid ohne Isonitrilverunreinigung.[7]
Propionitril wird entweder durch Hydrierung von Acrylnitril oder durch die Gasphasenreaktion von Propanal oder Propanol mit Ammoniak. Es fällt auch als Nebenprodukt bei der Elektrohydrodimerisierung von Acrylnitril zu Adiponitril an (EHD-Verfahren).[2]
Die Verbindung kann auch durch Erhitzen von Bariumethylsulfat und Kaliumcyanid mit anschließender Destillation oder durch Dehydratisierung von Propionsäure + Ammoniak oder Propionamid hergestellt werden.[4][8]
Allgemein lassen sich Nitrile wie Propionitril über die Kolbe-Nitrilsynthese herstellen, bei der in diesem Fall Ethanhalogenide (–Cl, –Br, –I) oder Ethyltoluol-4-sulfonat mit Alkalimetallcyaniden in polaren, aprotischen Lösungsmitteln (DMSO, Aceton) zur Reaktion gebracht werden.[9][10] Da es sich bei dem eingesetzten Cyanid um ein ambidentes Nucleophil handelt, entsteht zusätzlich auch das isomere Isonitril. Das Verhältnis von Nitril zu Isonitril ist dabei von dem Reaktionstyp und den Reaktionsbedingungen abhängig.[9]
Weitere Synthesewege zum Propionitril können mit der Hydrocyanierung als auch generell mit der katalytischen Oxidation von Kohlenwasserstoffen mit Luft in Gegenwart von Ammoniak beschritten werden. Im Falle von Propionitril führt letztere Methode vorerst nur zum Acrylnitril.
Eigenschaften
Propionitril ist eine farblose, leicht flüchtige, in Wasser leicht lösliche Flüssigkeit mit einem charakteristischen Geruch. Sie ist leicht entzündlich und die Dämpfe bilden mit der Luft explosive Gemische (3,1–14 %). Bei hohen Temperaturen zersetzt sich Propionitril unter anderem zu Blausäure und zu diversen Stickoxiden.[1]
Verwendung
Propionitril eignet sich gut für die Weiterreaktion über Hydrolyse zu Propionsäureamid und weiter zur Propionsäure, oder über Reduktion zu Propylamin.
Die Hydrierung von Propionitril ergibt N-Propylamine. Die Verbindung wird auch als Zwischenprodukt zur Herstellung anderer organischer Verbindungen verwendet, zum Beispiel bei der Synthese der Arzneimittel Flopropion (über die Houben-Hoesch-Reaktion) und Ketoprofen.[2]
Es wird auch als Lösungsmittel und in der organischen Synthese als Bindemittel für Harze eingesetzt.[4]
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu Propionitril in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. November 2021. (JavaScript erforderlich)
- ↑ a b c Peter Pollak, Gérard Romeder, Ferdinand Hagedorn, Heinz-Peter Gelbke: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag & Co. KGaA, Weinheim, Germany 2000, ISBN 978-3-527-30673-2, Nitriles, S. a17_363, doi:10.1002/14356007.a17_363.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-440.
- ↑ a b c Patty's Toxicology, 6 Volume Set. Wiley, 2012, ISBN 978-0-470-41081-3, S. 967 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Propionitril bei Merck, abgerufen am 19. Januar 2011.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-23.
- ↑ O. Reutov, A. L. Kurts: Ambident anions. Springer US, 1983, ISBN 978-0-306-10975-1, S. 211 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Nitrogen and Phosphorus Solvents. Elsevier Science, 2013, ISBN 978-1-4832-9020-1, S. 355 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b L. Friedman, Harold Shechter: Preparation of Nitriles from Halides and Sodium Cyanide. An Advantageous Nucleophilic Displacement in Dimethyl Sulfoxide 1a. In: The Journal of Organic Chemistry. Band 25, Nr. 6, 1960, ISSN 0022-3263, S. 877–879, doi:10.1021/jo01076a001 (acs.org).
- ↑ N. L. Allinger, et al.: Organische Chemie. [Hauptbd.] Walter de Gruyter, 2011, ISBN 978-3-11-082970-9, S. 604 (eingeschränkte Vorschau in der Google-Buchsuche).

