Rhenium(V)-chlorid
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
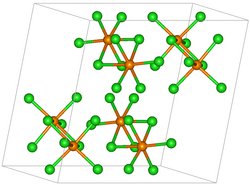
| |||||||||||||
| _ Re5+ _ Cl− | |||||||||||||
| Kristallsystem |
monoklin | ||||||||||||
| Raumgruppe |
P21/c | ||||||||||||
| Gitterparameter |
a = 924 pm, b = 1154 pm, c = 1203 pm, β = 109,1° | ||||||||||||
| Allgemeines | |||||||||||||
| Name | Rhenium(V)-chlorid | ||||||||||||
| Andere Namen |
Rheniumpentachlorid | ||||||||||||
| Verhältnisformel | ReCl5 | ||||||||||||
| Kurzbeschreibung |
dunkelgrüner Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 363,47 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Dichte |
3,9 g·cm−3[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||
| ΔHf0 | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Rhenium(V)-chlorid ist eine anorganische chemische Verbindung des Rheniums aus der Gruppe der Chloride.
Gewinnung und Darstellung
Rhenium(V)-chlorid kann durch Reaktion von Rhenium mit Chlor gewonnen werden.[4]
Es kann auch aus Rhenium(VII)-oxid und Tetrachlorkohlenstoff dargestellt werden.
Eigenschaften
Rhenium(V)-chlorid liegt in Form von paramagnetischen, an feuchter Luft unbeständigen, schwarzbraunen, grünlich schillernden Kristallen vor. Der Dampf ist ebenfalls dunkelbraun. Es besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14) und den Gitterparametern a = 924 pm, b = 1154 pm, c = 1203 pm und β = 109,1°. Die Kristallstruktur besteht aus Re2Cl10-Einheiten bei doppelt-hexagonaler Packung. Es ist löslich in Cyclohexan und reagiert mit Sauerstoff bei erhöhter Temperatur zu Rheniumoxidchloriden. Es reagiert mit Wasser zu HReO4 und schwarzem unlöslichen Rhenium(IV)-oxid bzw. grünem gelösten ReCl62−. In einer Chlor-Atmosphäre oder im Vakuum unzersetzt destillierbar, zerfällt oberhalb des Schmelzpunktes in Stickstoff oder Argon zu Rhenium(III)-chlorid und Chlor.[4]
Verwendung
Rhenium(V)-chlorid wird als Ausgangsmaterial für Rheniumporphyrine und Rheniumalkinkomplexen verwendet.[1]
Einzelnachweise
- ↑ a b c d e Datenblatt Rhenium(V) chloride bei Sigma-Aldrich, abgerufen am 25. Mai 2017 (PDF).
- ↑ a b Roger Blachnik (Hrsg.): Taschenbuch für Chemiker und Physiker. Band III: Elemente, anorganische Verbindungen und Materialien, Minerale. begründet von Jean d’Ans, Ellen Lax. 4., neubearbeitete und revidierte Auflage. Springer, Berlin 1998, ISBN 3-540-60035-3, S. 694 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ A. F. Holleman, N. Wiberg: Anorganische Chemie. 103. Auflage. 2. Band: Nebengruppenelemente, Lanthanoide, Actinoide, Transactinoide. Walter de Gruyter, Berlin / Boston 2016, ISBN 978-3-11-049590-4, S. 1921 (Leseprobe: Teil C – Nebengruppenelemente. Google-Buchsuche).
- ↑ a b Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1608.

