Lichtschutzmittel
Lichtschutzmittel sind Stoffe, die Organismen oder technische Produkte vor dem schädigenden Einfluss von Licht, insbesondere UV-Strahlung, schützen. Der schützende Effekt entsteht durch die Absorption, Reflexion oder Streuung der UV-Strahlung, wodurch weniger Strahlung auf oder in den zu schützenden Körper dringt. Für den Menschen hat vor allem die Sonnencreme Relevanz, welche durch ihre Anwendung vor Hautkrebs schützt.[1] Von Seiten der technischen Produkte seien hier Polymere und Lacke erwähnt, welche mit Lichtschutzmitteln, meist als Additive, versetzt werden.
UV-Absorber (UV-Filter)
UV-Absorber (Synonym „UV-Filter“) finden sich in Kosmetika – wie Sonnencremes – zum Schutz der Haut[2][3] oder in Gegenständen zum Schutz der Materialien. Die Konzentration an Filtersubstanzen hat direkten Einfluss auf den Lichtschutzfaktor.[4] Dieser Effekt gehorcht dem Prinzip der Lichtabsorption (Lambert-Beersches Gesetz). Die absorbierte Menge an UV-Strahlung ist dabei eine Funktion der Dicke des durchstrahlten Körpers (Der aufgebrachten Schicht) und der Konzentration des UV-Absorbers.[5] Sie wird als thermische Energie wieder abgegeben.
In Europa zugelassene UV-Absorber sind in der deutschen Kosmetik-Verordnung aufgeführt. Da die einzelnen Substanzen in der Regel keinen Schutz über das gesamte UV-Spektrum hinweg bieten, werden meist mehrere Stoffe kombiniert, da sich die Effekte verschiedener UV-Absorber ergänzen. Der UV-Absorber dient als Beschichtung und zieht teilweise in die Hornschicht der Haut ein.
Die Wirkung des UV-Absorbers beruht bei absorbierter UV-Strahlung auf der Stokes-Verschiebung, bei organischen UV-Absorbern erfolgt die Stokes-Verschiebung aufgrund von konjugierten Doppelbindungen. Nach ihrem Absorptionsspektrum unterscheidet man UVA-, UVB- und Breitbandfilter (UVA-/UVB-Absorber). Organische UV-Absorber sind oftmals Derivate von Campher, Salicylsäure (z. B. Homosalat) oder Zimtsäure. Anorganische UV-Absorber sind z. B. feinteilige Titandioxid- und Zinkoxid-Partikel. Da diese UV-Absorber über ihre Sichtbarkeit eine Auftragskontrolle ermöglichen, werden sie häufig in Kinderprodukten eingesetzt. Eine Alternative zu UV-Absorbern sind textile Bedeckungen wie Kleidung oder bedingt der Aufenthalt im Schatten, wobei über die Reflexion trotzdem UV-Strahlung auf die Haut trifft.
Darüber hinaus kommen UV-Absorber, wie Benzotriazole, auch allgemein beim Materialschutz zum Einsatz.

In Lacken kann nanoskaliges Titandioxid als anorganischer UV-Absorber eingesetzt werden.[7] Im Gegensatz zu dem als Pigment eingesetzten, gröberen Titandioxid sind sehr feine Typen transparent und verursachen so keine Trübung des Lacks. Insbesondere nicht nachbehandelte Titandioxidpigmente sind dagegen Hauptbestandteil des Kreidungszyklus und damit ein Hauptgrund für das Schadensbild der Kreidung.[8] Eisenoxidpigmente wirken dagegen ausschließlich als UV-Absorber, können aber aufgrund ihrer Eigenfarbe nicht in allen Anwendungen verwendet werden.[9]
Bei Lebensmittelverpackungen können Zinkoxid-Nanopartikel als UV-Absorber in eingesetzt. Werden Zinkoxid-Nanopartikel dabei auf diese Lebensmittel übertragen, kann der Konsum zu Veränderungen des Darms und einer Verringerung der Nährstoffaufnahme führen.[10]
Arten von UV-Absorbern
Organische UV-Absorber:[11]
- 2-(2-Hydroxyphenyl)-2H-benzotriazole (z. B. 2-(2H-Benzotriazol-2-yl)-4,6-bis(2-phenyl-2-propanyl)phenol und 2-(2H-Benzotriazol-2-yl)-4,6-di-tert-butylphenol)
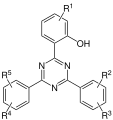
- (2-Hydroxyphenyl)-s-triazine
- Hydroxybenzophenone
- Oxalanilide
- 2-(2-Hydroxyphenyl)-2H-benzotriazole.svg
Allgemeine Struktur von 2-(2-Hydroxyphenyl)-2H-benzotriazolen
- Hydroxybenzophenone.svg
Allgemeine Struktur von Hydroxybenzophenonen
Allgemeine Struktur von Oxalaniliden
Anorganische UV-Absorber:
- Titandioxid
- Eisenoxidpigmente
- Zinkoxid
- Verbindungen (beispielsweise Stearate wie Cadmiumstearat) auf Basis von Blei, Cadmium Zinn, Barium/Zink, Calcium/Zink und Calcium/Aluminium/Zink[12]
Kritik
Manche üblicherweise eingesetzten Substanzen, wie z. B. Benzophenon-4, 3-Benzylidencampher (3-BC), 4-Methylbenzylidencampher, haben aber auch eine hormonartige (östrogene, d. h. verweiblichende) Wirkung, weshalb sie als Umweltchemikalien gelten und zu den endokrinen Disruptoren gezählt werden.[13][14] So verursacht 3-BC bei Fischen (z. B. in Männchen von Pimephales promelas) ab einer Konzentration von 73 µg/L die Bildung des Eidotterproteins Vitellogenin (VTG).[15] VTG gilt in der Ökotoxikologie als zuverlässiger Biomarker für Verweiblichung.
Zinkoxid-UV-Absorber basieren auf Nanopartikeln mikrofeinen Zinkoxids. Während solche UV-Absorber in der Schweiz nicht zugelassen sind, hat das deutsche Bundesinstitut für Risikobewertung (BfR) bisher keine gesundheitlichen Bedenken, wenn Sonnenschutzmittel höchstens 25 % mikrofeines Zinkoxid enthalten. Das BfR stellt allerdings fest, dass diese Partikel in geringen Mengen in die Haut eindringen können.[16] Zink, das von Zinkoxid-Partikeln stammt, konnte in geringen Mengen in Blut und Urin nachgewiesen werden.[17]
In den Vereinigten Staaten wird kritisiert, dass der Bevölkerung der Zugang zu in Europa zugelassenen UV-Absorbern wie beispielsweise Amiloxat, Bemotrizinol, Iscotrizinol oder Octyltriazon verwehrt werde, so dass die steigenden Hautkrebsraten nur ungenügend bekämpft werden können.[18]
Radikalfänger
Radikalfänger dienen nicht der Absorption der UV-Strahlung, sondern verringern die Schäden, welche durch UV-Strahlung entstehen. Hierbei handelt es sich i. d. R. um Radikale, welche bei der Aufspaltung von chemischen Bindungen, durch UV-Strahlung, entstehen. Die größte Gruppe der Radikalfänger sind die sogenannte Hindered Amine Light Stabilizers (HALS).
Hindered Amine Light Stabilizers
Hindered Amine Light Stabilizers (HALS, Übersetzung in etwa: sterisch gehinderte Amine als Lichtschutzmittel) sind chemische Verbindungen, die Amine als funktionelle Gruppe enthalten und die als UV-Stabilisatoren in Polymeren (Kunststoffen) und Lacken bzw. Beschichtungen verwendet werden.[19] Diese Verbindungen sind typischerweise Derivate von Tetramethylpiperidin und werden hauptsächlich verwendet, um die Polymere vor den Auswirkungen von Photooxidation zu schützen, im Gegensatz zu anderen Formen von Polymerabbau wie Ozonolyse.[20][21]
HALS werden auch zunehmend als thermische Stabilisatoren eingesetzt,[22] insbesondere für niedrige und moderate Wärmemengen, bleiben jedoch während der Hochtemperaturverarbeitung von Polymeren (z. B. Spritzgießen) weniger wirksam als herkömmliche phenolische Antioxidantien.[23]
Neben dem Einsatz im Bereich des Spritzgießens von Polymeren finden HALS auch Einsatz in Lacken und anderen Beschichtungsstoffen. Hier dienen sie vor allem dazu, den Lacken eine ausreichende Bewitterungsstabilität (v.A. ggü. Sonneneinstrahlung) zu verleihen.[24]
Wirkungsmechanismus von HALS
HALS absorbieren keine UV-Strahlung, sondern hemmen den Abbau des Polymers durch kontinuierliches und zyklisches Entfernen von Radikalen, die durch Photooxidation des Polymers entstehen. Der Gesamtprozess wird manchmal als Denisov-Zyklus bezeichnet, nach Jewgeni Timofejewitsch Denissow[25] und ist äußerst komplex.[26] Häufig reagieren HALS mit den durch die Reaktion von Polymer und Sauerstoff gebildeten Ausgangspolymerperoxyradikalen (ROO •) und Alkylpolymerradikalen (R •), wodurch eine weitere radikalische Oxidation verhindert wird. Durch diese Reaktionen werden HALS zu ihren entsprechenden Aminoxylradikal (R2NO• c.f. TEMPO) oxidiert, sie können jedoch über eine Reihe von zusätzlichen Radikalreaktionen zu ihrer ursprünglichen Aminform zurückkehren. Die hohe Effizienz und Langlebigkeit von HALS beruht auf diesem zyklischen Prozess, bei dem die HALS während des Stabilisierungsprozesses regeneriert und nicht verbraucht werden.
Die Verwendung eines gehinderten Amins, das keine alpha-Wasserstoffatome besitzt, verhindert, dass das HALS in ein Nitron umgewandelt wird. Die Bildung des Nitrons kann entweder durch dimerisieren oder mit einer beliebigen Alkengruppen im Polymer (Nitrone-olefin (3+2) cycloaddition) geschehen, wodurch das HALS inaktiviert wird.
Obwohl HALS in Polyolefinen, Polyethylenen und Polyurethanen äußerst wirksam sind, sind sie in Polyvinylchlorid (PVC) unwirksam. Es wird angenommen, dass ihre Fähigkeit, Nitroxylradikale zu bilden, dadurch beeinträchtigt wird, dass sie leicht durch HCl, die durch Dehydrohalogenierung von PVC freigesetzt wird, protoniert wird.
Beispiele für HALS
- 2,2,6,6-Tetramethylpiperidin-Derivate wie Bis(2,2,6,6-tetramethyl-4-piperidyl)sebacat (Tinuvin® 770)
Anwendungen
Bei der Verwendung von Lichtschutzmitteln sind Kunststoffe (insbesondere Elastomere, wie Gummi), Textilien und Anstrichmittel schutzbedürftig.[27] Es kommt oftmals eine Kombination aus UV-Absorbern und Radikalfänger zum Einsatz. Der Einsatz von UV-Absorbern ist notwendig um die Schicht bzw. das darunter liegende Bauteil oder die Menschliche Haut vor der UV-Strahlung zu schützen. Da es jedoch in einer dünnen Schicht an der Oberfläche, z. B. eines Lackes, noch zu keiner ausreichenden Absorption der UV-Strahlung gekommen ist, ist hier zusätzlich der Einsatz der Radikalfänger notwendig.
Kunststoffe
Kunststoffe sind bei Lichteinwirkung durch Photolyse einer Photooxidation unterworfen. Dabei entstehen verschiedene Radikale, die das Material angreifen. Durch diese werden die Hauptketten des Polymers aufgebrochen und verschiedene polare Verbindungen, wie zum Beispiel Peroxide, eingebaut. Die Folgen dieses Abbaus sind Farbverluste, Rissbildung und generell negative Auswirkungen auf die physikalisch mechanischen Eigenschaften.[28]
Lacke
In Lacken werden UV-Absorber und Radikalfänger zur Verbesserung der Bewitterungsstabilität eingesetzt. Insbesondere in Klarlacken ist es wichtig, dass die eingesetzten UV-Stabilisatoren farblos sind und keiner Farbveränderung unterliegen. Aufgrund der Neigung zur Migration wird in Zweischichtsystemen auch der Basislack mit UV-Stabilisatoren ausgestattet, obwohl dieser durch einen stabilisierten Decklack bereits vor ultravioletter Strahlung geschützt wird.[29] Für Metallicbeschichtungen von Automobilen kann die Beständigkeit von Farbe, Glanz und Rissbeständigkeit, bei geschicktem Einsatz von HALS und UV-Absorbern, für Zeiträume von mehr als 10 Jahren garantiert werden.[30]
Schutz menschlicher Haut
Die zum Schutz menschlicher Haut verwendeten Lichtschutzmittel werden meist Sonnenschutzmittel genannt.[31] Sie sollen die schädigende Wirkung von Sonnenstrahlen oder künstlicher UV-Bestrahlung auf die Haut unterbinden.
Siehe auch
Weblinks
- UV-light stabilizers Hindered amine light stabilizers (englisch)
- flexorb Gas treating (englisch)
Weiterführende Literatur
- Streitberger, Hans-Joachim; Goldschmidt, Artur: BASF Handbuch Lackiertechnik. ISBN 978-3-86630-892-3.
- Valet, Andreas: Lichtschutzmittel. ISBN 978-3-87870-437-9.
- Müller, Bodo: Lackadditive Kompakt erklärt. ISBN 978-3-86630-695-0.
- Johannes Karl Fink: A Concise Introduction to Additives for Thermoplastic Polymers. ISBN 0-470-60955-9.
Einzelnachweise
- ↑ U. Leiter, C. Garbe: Epidemiology of melanoma and nonmelanoma skin cancer–the role of sunlight. In: Advances in Experimental Medicine and Biology. Band 624, 2008, S. 89–103; doi:10.1007/978-0-387-77574-6_8. PMID 18348450.
- ↑ G. J. Nohynek, H. Schaefer: Benefit and risk of organic ultraviolet filters. In: Regulatory Toxicology and Pharmacology. Band 33, Nummer 3, Juni 2001, S. 285–299; doi:10.1006/rtph.2001.1476. PMID 11407932.
- ↑ N. A. Quatrano, J. G. Dinulos: Current principles of sunscreen use in children. In: Current Opinion in Pediatrics. Band 25, Nummer 1, Februar 2013, S. 122–129; doi:10.1097/MOP.0b013e32835c2b57. PMID 23295720.
- ↑ L. Scherschun, H. W. Lim: Photoprotection by sunscreens. In: American Journal of Clinical Dermatology. Band 2, Nummer 3, 2001, S. 131–134, ISSN 1175-0561. PMID 11705089.
- ↑ Ultraviolet Absorbers (Memento vom 2. Mai 2009 im Internet Archive).
- ↑ T. Werner: Triplet deactivation in benzotriazole-type ultraviolet stabilizers. In: The Journal of Physical Chemistry. Band 83, Nr. 3, 1979, S. 320–325, doi:10.1021/j100466a004.
- ↑ hessen-nanotech.de: Schutz vor Strahlung und Temperatureinflüssen – UV-Schutzschichten, abgerufen am 12. April 2013.
- ↑ J. Winkler; Titandioxid; Vincentz Network; Hannover; 2003; ISBN 3-87870-738-X
- ↑ G. Buxbaum, G. Pfaff; Industrial Inorganic Pigments; 3. Auflage; Wiley-VCH; Weinheim; 2005; ISBN 3-527-30363-4
- ↑ Fabiola Moreno-Olivas, Elad Tako und Gretchen J. Mahler: ZnO nanoparticles affect intestinal function in an in vitro model. In: Food & Function. 2018, doi:10.1039/C7FO02038D.
- ↑ Eintrag zu UV-Absorber. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Januar 2020.
- ↑ Gesamtbericht Behandlungs- und Verwertungswege für PVC-Abfälle; Bundesministerium für Land- und Forstwirtschaft, Umwelt und Wasserwirtschaft, Wien, Dezember, 2002, (PDF-Datei)
- ↑ UV-Filter in Kosmetika und im Materialschutz. In: Karl Fent: Ökotoxikologie. 4., vollständig überarbeitete Auflage. Stuttgart 2013, ISBN 978-3-13-109994-5, S. 309f.
- ↑ Margret Schlumpf u. a.: Estrogenic activity and estrogen receptor beta binding of the UV filter 3-benzylidene camphor. Comparison with 4-methylbenzylidene camphor. In: Toxicology. 199, 2004, S. 109–120. PMID 15147785.
- ↑ Tab. 9.9, Wirkungen estrogener Umweltstoffe auf Fische in vivo sowie PNEC-Werte. In: Karl Fent: Ökotoxikologie. 4., vollständig überarbeitete Auflage. , Stuttgart 2013, ISBN 978-3-13-109994-5, S. 306.
- ↑ Sonnenschutzmittel: Zinkoxid als UV-Filter ist nach derzeitigem Kenntnisstand gesundheitlich unbedenklich. (PDF; 44 kB) Stellungnahme Nr. 037/2010 des BfR vom 18. Juni 2010.
- ↑ B. Gulson, M. McCall, M. Korsch, L. Gomez, P. Casey, Y. Oytam, A. Taylor, M. McCulloch, J. Trotter, L. Kinsley, G. Greenoak: Small amounts of zinc from zinc oxide particles in sunscreens applied outdoors are absorbed through human skin. In: Toxicological Sciences. 118 (1), 2010, S. 140–149. doi:10.1093/toxsci/kfq243.
- ↑ Marc S. Reisch: After More Than A Decade, FDA Still Won’t Allow New Sunscreens. In: Chemical & Engineering News. 93(20), 2015, S. 10–15.
- ↑ Hans Zweifel, Ralph D. Meier, Michael Schiller: Plastics additives handbook. 6. Auflage. Hanser, München 2009, ISBN 978-3-446-40801-2.
- ↑ Klaus Köhler, Peter Simmendinger, Wolfgang Roelle, Wilfried Scholz, Andreas Valet, Mario Slongo: Paints and Coatings, 4. Pigments, Extenders, and Additives. In: Ullmann's Encyclopedia Of Industrial Chemistry. 2010, doi:10.1002/14356007.o18_o03.
- ↑ Pieter Gijsman: Photochemistry and Photophysics of Polymer Materials Photochemistry. John Wiley & Sons, Hoboken, doi:10.1002/9780470594179.ch17.
- ↑ Pieter Gijsman: A review on the mechanism of action and applicability of Hindered Amine Stabilizers. In: Polymer Degradation and Stability. 145, November 2017, S. 2–10. doi:10.1016/j.polymdegradstab.2017.05.012.
- ↑ R Gensler, C.J.G Plummer, H.-H Kausch, E Kramer, J.-R Pauquet, H Zweifel: Thermo-oxidative degradation of isotactic polypropylene at high temperatures: phenolic antioxidants versus HAS. In: Polymer Degradation and Stability. 67, Nr. 2, Februar 2000, S. 195–208. doi:10.1016/S0141-3910(99)00113-5.
- ↑ Streitberger, Hans-Joachim; Goldschmidt, Artur: BASF Handbuch Lackiertechnik. Hrsg.: Vincentz. 2. Aufl., rev. Ausg. Vincentz Network, Hannover 2014, ISBN 978-3-86630-892-3, S. 194.
- ↑ E.T. Denisov: The role and reactions of nitroxyl radicals in hindered piperidine light stabilisation. In: Polymer Degradation and Stability. 34, Nr. 1–3, Januar 1991, S. 325–332. doi:10.1016/0141-3910(91)90126-C.
- ↑ Jennifer L. Hodgson, Michelle L. Coote: Clarifying the Mechanism of the Denisov Cycle: How do Hindered Amine Light Stabilizers Protect Polymer Coatings from Photo-oxidative Degradation?. In: Macromolecules. 43, Nr. 10, 25. Mai 2010, S. 4573–4583. bibcode:2010MaMol..43.4573H. doi:10.1021/ma100453d.
- ↑ Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 3: H–L. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1983, ISBN 3-440-04513-7, S. 2363–2364.
- ↑ Ultraviolet Absorbers (Memento vom 2. Mai 2009 im Internet Archive).
- ↑ A. Goldschmidt, H. Streitberger: BASF Handbuch Lackiertechnik. Vincentz Network, Hannover 2002, ISBN 3-87870-324-4, S. 191 ff.
- ↑ Streitberger, Hans-Joachim; Goldschmidt, Artur: BASF Handbuch Lackiertechnik. Hrsg.: Vincentz. 2. Aufl., rev. Ausg. Vincentz Network, Hannover 2014, ISBN 978-3-86630-892-3, S. 194.
- ↑ Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 1310.