Desulfovibrionales
| Desulfovibrionales | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
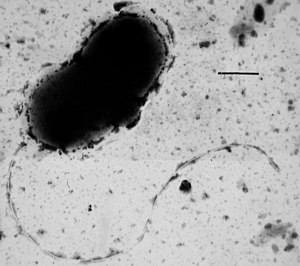
Desulfovibrio vulgaris | ||||||||||
| Systematik | ||||||||||
| ||||||||||
| Wissenschaftlicher Name | ||||||||||
| Desulfovibrionales | ||||||||||
| Kuever et al., 2006 |
Die Desulfovibrionales bilden eine Ordnung innerhalb der Deltaproteobacteria. Mit Ausnahme von Lawsonia und Bilophila können alle Arten dieser Ordnung durch anaerobe Atmung Sulfat reduzieren. Bakterien mit dieser Eigenschaft werden als Desulfurizierer bezeichnet. Sie spielen durch die Bildung von Schwefelwasserstoff aus Sulfat eine wichtige Rolle im Schwefelkreislauf. Die Zellform ist stäbchenförmig oder auch gekrümmt, meist tragen sie Geißeln. Wie alle Proteobakterien sind sie gramnegativ.
Ökologie und Vorkommen
Viele Arten dieser Ordnung sind mesophil, d. h. sie benötigen für das Wachstum Temperaturen zwischen 30 und 40 Grad. Auch thermophile Mitglieder bei Temperaturen zwischen 50 und 60 Grad sind vorhanden, einige Arten wurden in geothermischen Umgebungen im Meer gefunden. Diese Ordnung ist in fast allen aquatischen Habitaten (Meer, Süßwasser, Grundwasser) vertreten. In der Regel kommen diese Organismen in Umgebungen mit neutralen pH-Wert vor. Wenige wie Desulfonatronovibrio sind auch alkaliphil, sie benötigen hohe pH-Werte für das Wachstum.
Lawsonia (Desulfovibrionaceae) zählt nicht zu den Desulfurizierern. Diese Gattung ist ein obligat interzellulärer Parasit, gefunden in Darmzellen von Schweinen. Bilophila zählt ebenfalls nicht zu den Sulfat-reduzierenden Bakterien, es wurde u. a. in Patienten mit Blinddarmentzündungen gefunden.
Die Bedeutung der sulfatreduzierenden Bakterien für den Schwefelkreislauf in der Natur ist enorm. Der größte Anteil des Schwefelwasserstoffes wird durch die Sulfatatmung gebildet. Das große Vorkommen von Schwefelablagerungen in Louisiana und an der Golfküste Texas wurde wahrscheinlich von verschiedenen Sulfatatmern, wie Desulfovibrio desulfuricans erzeugt.
Stoffwechsel und Desulfurikation
Fast alle Bakterien der Desulfovibrionales sind Fermentierer. Häufige organische Verbindungen, die häufig fermentiert werden, sind u. a. Fumarat, Malat und Pyruvat. Es besteht eine große Vielfalt von Stoffen, die fermentiert werden können. Beispielsweise fermentiert Desulfovibrio aminophilus u. a. Threonin und Glycin.
Der Name Desulfovibrionales deutet auf die Desulfurikation hin. Bei der Desulfurikation spricht man auch von Sulfatatmung oder dissimilatorischer Sulfatreduktion. Entsprechende Bakterien werden als Desulfurikanten, Sulfatatmer oder Sulfatreduzierer (engl.: sulfate reducing bacteria, SRB; bzw. sulfate reducing prokaryotes, SRP) bezeichnet. Bei der Sulfatatmung wird Sulfat (SO42−) zu Schwefelwasserstoff (H2S) reduziert. Bei dieser Form des oxidativen Energiestoffwechsels ist nicht Sauerstoff wie bei der aeroben Atmung, sondern Sulfat, Sulfit oder Thiosulfat der Elektronenakzeptor. Einfache organische Verbindungen oder elementarer, molekularer Wasserstoff (H2) dienen als Donatoren, sie werden oxidiert. Die entsprechenden Schwefelverbindungen werden hierbei zu Sulfiden bzw. Schwefelwasserstoff reduziert. Organische Stoffe werden meist nicht vollständig oxidiert, sondern Acetat ist das Endprodukt. Vollständige Oxidation mit CO2 als Endprodukt ist seltener (z. B. bei Desulfothermus naphthaee).
Bei der Sulfatreduktion wird im Allgemeinen zunächst aus Sulfat und Adenosintriphosphat (ATP) unter Abspaltung von Diphosphat (Pyrophosphat) Adenosinphosphosulfat (APS) gebildet. Im weiteren Schritt wird hieraus mit Hilfe des Enzyms APS–Reduktase unter Reduktion Adenosinmonophosphat (AMP) und Sulfit gebildet. Sulfit wird dann zu H2S reduziert. Dazu werden die dissimilatorischen Sulfitreduktasen (dSiRs) eingesetzt. Bei den Desulfovibrionales handelt es sich meist um das Enzym Desulfoviridin. Andere dSiRs sind Desulforubidin (hauptsächlich bei der Ordnung Desulfobulbaceae, auch bei Desulfomicrobium norvegicum nachgewiesen), P582 (z. B. bei Desulfotomaculum nigrificans, ein grampositives Bakterium der Clostridiales) und Desulfofuscidin (z. B. bei Thermodesulforhabdus der Syntrophobacteraceae).
Die Sulfatreduktion wird bei den als Sulfatatmer bezeichneten Bakterien als „dissimilativ“ bezeichnet, obwohl es sich nicht um eine Dissimilation handelt (es werden keine Organismenbestandteile abgebaut). Im Gegensatz zur assimilativen Sulfatreduktion (Sulfatassimilation) dient die Reduktion von Schwefelverbindungen bei den Desulfurikanten (Sulfatatmern) ausschließlich der Energiegewinnung. Dagegen dient die assimilatorische Sulfatreduktion, zu der fast alle Bakterien und auch viele Eukaryonten (die meisten Pflanzen und Pilze; Tiere allerdings nicht) fähig sind, dem Aufbau von schwefelhaltigen Organismenbestandteilen, beispielsweise Aminosäuren, im Gegensatz zur Sulfatreduktion der Desulfurikanten, die den durch die Reduktion entstehenden Schwefelwasserstoff sofort ausscheiden.
Bilophila (Desulfovibrionaceae) wurde u. a. im Verdauungstrakt von Menschen gefunden. Sie kann nicht Sulfat reduzieren, sondern benötigt organische Schwefelquellen wie Taurin. Hieraus kann Sulfit gewonnen werden. Sulfit wird wiederum durch ein Enzym, eine dissimilatorische Sulfit-Reduktase (dSIR, bzw. DSR) zu Sulfid reduziert.[1] Das genutzte Enzym ähnelt stark dem von Desulfovibrio (Desulfoviridin). Da Bilophila nicht in der Lage ist, anorganisches Sulfat zu nutzen, wird sie nicht zu den Desulfurikanten gestellt. Es wird angenommen, dass während der Evolution die Fähigkeit zur Desulfurikation verloren gegangen ist.
Die dissimilatorische Sulfatreduktion ist ein Kennzeichen für diese Ordnung aber auch der Desulfobacterales und Syntrophobacterales innerhalb der Deltaproteobacteria. Weiterhin gibt es diesen Stoffwechselweg auch bei den Thermodesulfobacteria und bei der grampositiven Ordnung Clostridiales (Gattung Desulfotomaculum). Auch in der Domäne Archaea (z. B. Archaeglobus) gibt es Desulfurizierer.
Eisen, Mangan und andere Elektronenakzeptoren
Auch dreiwertiges Eisen (Fe3+) kann bei verschiedenen Arten der Desulfovibrionales als alternativer Elektronenakzeptor bei der anaeroben Atmung dienen. Fe3+ wird hierbei zu Fe2+ reduziert. Desulfovibrio desulfuricans nimmt z. B. das dreiwertige Eisenion in Form von Eisen(III)-chlorid auf. Als Donator dient Lactat.
Manganreduktion tritt ebenfalls bei verschiedenen Mitgliedern auf. Zum Beispiel reduzieren Desulfovibrio desulfuricans und Desulfomicrobium baculatum Mn(IV) zu Mn(II).
Einige Arten dieser Ordnung können auch Nitrat als Elektronenakzeptor verwenden: Desulfovibrio desulfuricans reduziert beispielsweise Nitrat zu Ammoniak. Bei der Gattung Desulfovibrio wurde die Fähigkeit, Uran als Elektronenakzeptor zu verwenden, nachgewiesen: U(VI) wird zu U(IV) reduziert. Desulfovibrio vulgaris verwendet Cytochrom-c3 als Uran-Reduktase.[2] Wenn U(VI) als einziger für das Bakterium nutzbarer Elektronenakzeptor vorliegt, wurde allerdings kein Wachstum beobachtet.[3] Ein Bakterium, welches U(VI) als einzigen Elektronenakzeptor nutzen kann und dabei auch Wachstum zeigt, ist z. B. Geobacter metallireducens der Geobacteraceae.[4] Auch Shewanella putrefaciens, eine Bakterienart der Gammaproteobacteria, zeigt diese Fähigkeit.
Disproportionierung
Einige Arten der Desulfovibrionales sind Disproportionierer. Bei der Disproportionierung werden Schwefelverbindungen wie Thiosulfat oder Sulfit zu Sulfat und Sulfid (Schwefelwasserstoff) umgesetzt. Der dabei entstehende Protonengradient wird zur Produktion von ATP eingesetzt. Einige Arten der Desulfovibrionales nutzen diesen Weg, beispielsweise wächst Desulfovibrio oxyclinae und Desulfovibrio cuneatus, wenn Acetat vorhanden ist, durch die Disproportionierung von Sulfit und Thiosulfit. Weitere Disproportionierer sind Desulfovibrio aminophilus und eventuell Desulfonatronovibrio.
Desulfurizierer und Sauerstoff
Bis in die 80er Jahre wurden alle Sulfat reduzierenden Bakterien als obligat anaerob angesehen, also nur unter Ausschluss von Sauerstoff lebensfähig. Diese Ansicht hat sich in den letzten Jahren geändert.[5] Bei einigen wenigen Arten wurde in Kulturen eine geringe Sauerstofftoleranz (mikroaerob) festgestellt. So ist die Art Desulfovibrio oxyclinae auch in der Lage, mikroaerob zu wachsen und dabei sogar Sauerstoff als Elektronenakzeptor für das Wachstum zu nutzen. Die Sauerstofftoleranz und Nutzung von Desulfovibrio wurde in den letzten Jahren besonders untersucht.[6]
Auch in den oxischen Zonen von Bakterienmatten der Cyanobakterien, wo durch die Photosynthese hohe Sauerstoffkonzentrationen herrschen, wurden Sulfatreduzierer wie z. B. Desulfovibrio gefunden. Dort wurde auch eine hohe Sulfatreduktionsrate nachgewiesen.[7]
Systematik
Zu dieser Ordnung gehören folgende Familien und Gattungen (Auswahl):[8]
- Desulfovibrionaceae Kuever et al. 2006
- Desulfovibrio Kluyver and van Niel 1936
- Bilophila Baron et al. 1990
- Desulfocurvus Desulfocurvus Klouche et al. 2009
- Lawsonia McOrist et al. 1995
- Desulfohalobiaceae Kuever et al. 2006
- Desulfohalobium Ollivier et al. 1991
- Desulfohalophilus Blum et al.
- Desulfonatronospira Sorokin et al. 2008
- Desulfonatronovibrio Zhilina et al. 1997
- Desulfonauticus Audiffrin et al. 2003
- Desulfothermus Kuever et al. 2006
- Desulfovermiculus Belyakova et al. 2007
- Desulfomicrobiaceae Kuever et al. 2006
- Desulfomicrobium Rozanova et al. 1994
- Desulfonatronospira Sorokin et al. 2008
- Desulfonatronospira delicata Sorokin et al. 2008
- Desulfonatronumaceae Kuever et al. 2006
- Desulfonatronum Pikuta et al. 1998
Quellen
- ↑ Heike Laue, Michael Friedrich, Jürgen Ruff, Alasdair M. Cook: Dissimilatory Sulfite Reductase (Desulfoviridin) of the Taurine-Degrading, Non-Sulfate-Reducing Bacterium Bilophila wadsworthia RZATAU Contains a Fused DsrB-DsrD Subunit. In: Journal of Bacteriology. March 2001, Vol. 183, No. 5, S. 1727–1733.
- ↑ D. R. Lovley, P. K. Widman, J. C. Woodward, E. J. Phillips: "Reduction of Uranium by Cytochrome c3 of Desulfovibrio vulgaris", in: Appl. Environ. Microbiol. 1993, 59 (11), 3572–3576; PMID 8285665, PMC 182500 (freier Volltext).
- ↑ D. R. Lovley, E. J. Phillips: "Reduction of Uranium by Desulfovibrio desulfuricans", in: Appl. Environ. Microbiol. 1992, 58 (3), 850–856; PMID 1575486; PMC 195344 (freier Volltext).
- ↑ D. R. Lovley, E. J. P. Phillips, Y. A. Gorby, E. R. Landa: "Microbial Reduction of Uranium", in: Nature 1991, 350, 413–416; doi:10.1038/350413a0.
- ↑ L. K. Baumgartner, R.P. Reid, C. Dupraz, A. W. Decho, D. H. Buckley, J. R. Spear, K. M. Przekop, P. T. Visscher: Sulfate reducing bacteria in microbial mats: Changing paradigms, new discoveries. In: Sedimentary Geology. 185 (2006): S. 131–145. PDF (Memento des Originals vom 30. September 2007 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Heribert Cypionka: Oxygen respiration by Desulfovibrio species. In: Annual review of microbiology. 2000, vol. 54, pp. 827–848 (126 ref.)
- ↑ Waltraud Dilling, Heribert Cypionka: Aerobic respiration in sulfate-reducing bacteria. In: FEMS Microbiology Letters. 71 (1–2), 123–127 (1990). doi:10.1111/j.1574-6968.1990.tb03809.x.
- ↑ National Center for Biotechnology Information (NCBI) sowie J.P. Euzéby: List of Prokaryotic names with Standing in Nomenclature (LPSN). ( Systematik: Ordnung Desulfovibrionales (Memento des Originals vom 5. April 2011 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.)Stand: 23. Dezember 2012
Literatur
- Michael T. Madigan, John M. Martinko, Jack Parker: Brock – Mikrobiologie. 11. Auflage. Pearson Studium, München 2006, ISBN 3-8274-0566-1.
- George M. Garrity: Bergey's manual of systematic bacteriology. 2. Auflage. Springer, New York 2005, Vol. 2: The Proteobacteria Part C: The Alpha-, Beta-, Delta-, and Epsilonproteabacteria. ISBN 0-387-24145-0.
- Martin Dworkin, Stanley Falkow, Eugene Rosenberg, Karl-Heinz Schleifer, Erko Stackebrandt (Hrsg.): The Prokaryotes, A Handbook of the Biology of Bacteria. 7 Bände, 3. Auflage, Springer-Verlag, New York u. a. O. 2006, ISBN 0-387-30740-0. Vol. 2: Ecophysiology and Biochemistry. ISBN 0-387-2549-27.
Weblinks
- LPSN List of Prokaryotic Names with Standing in Nomenclature - Desulfovibrionales
- Labome.Org Eine Liste von Informationen, wissenschaftlichen Publikationen, Links...